Inscription / Connexion Nouveau Sujet
formule de lewis
Bonsoir à tous j'ai un exercice et j'aimerai une vérification de votre part:
on me demande de proposer une formule de lewis pour les éléments suivants et préciser leur structure tridimensionnelle grâce à la méthode du VSEPR
voici les éléments
SF2 , SF3+, SF6
pour F
SF2: j'ai mis
F-S-F
avec 3 doublet non liants sur les F (et je ne sais pas s'i faut mettre 2 doublets non liants sur le soufre)
SF3+: j'ai mis mis molécule entre crochet avec un moins []-
SF6 j'ai entouré S de F à une liaison chacun avec 3 doublets non liants pr chaque fluor
voila mercii
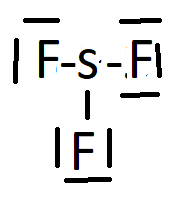
F est un halogène donc 2s2 2p5 3 doublets propres et un célibataire ne peut donner qu'une seule liaison !
S est en dessous de O donc 3s2 3p4 deux 2 doublets et deux célibataires à l'état fondamental mais existence de la couche 3d donc possibilité d'avoir jusqu'à 6 célibataires
SF6 6 liaisons simples type AX6 double pyramide à base carrée angles 90°
SF2 idem H2O AX2E2 géométrie tétrarédrique deux sommets occupés
angle 109,5° idéal mais F très électronégatif donc attire électron et "grossit" les angles augmentent
SF3 + électrons 6+3*7-1= 26 = 13doublets = 3*4+1
type AX3E1 tétraédrique comme SF2 2 sommets du tétraèdre occupés un peu plus symétrique comme NH3


