Inscription / Connexion Nouveau Sujet
Dosage par Titrage
Bonjour,
J'aimerai de l'aide concernant ces questions s'il vous plaît, merci.
On se propose de vérifier une valeur de concentration indiquée par un fabriquant en utilisant un dosage par titrage pH-métrique.
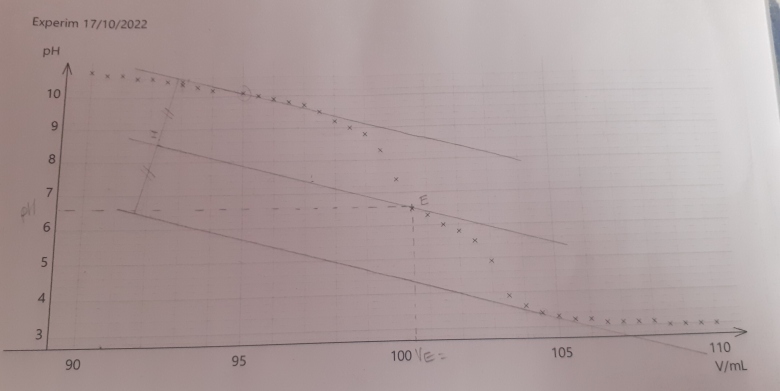
1) Déterminer le volume équivalent notée Ve.
J'ai utilisé la méthode des tangentes.
2) Etablir l'équation de la réaction support du titrage. Pour le titrage réalisé les couples acide/base sont : H3O+ / H2O ; H2O / HO-
H3O+ + HO- --> H20 + H20
3) Exprimer la quantité notée n0 d'hydroxyde de sodium initialement dans le bécher en fonction de Cd et Vd
4) Exprimer la quantité notée nA, d'acide chlorydrique apportée à l'équivalence en fonction de CA et de VE
5) En déduire alors la relation qui existe à l'équivalence
6) Calculer la concentration CD en hydroxyde de sodium de la solution diluée. En déduire la concentration C0 de la solution commerciale de Destop.
7) Déterminer la concentration massique C0 de la solution commerciale S0
8) L'indication du fabricant " solution à 10%" est-elle vérifiée ?
Aide : Pour cela, on pourra déterminer la masse d'hydroxyde de sodium présent dans 100 mL de Destop, puis pour 100g de Destop.
Données : La solution de DESTOP a été diluée 100 fois afin d'obtenir une solution Sd de concentration Cd
1mL de DESTOP, fiole jaugée de 100 mL
On a introduit 10,0 mL de la solution Sd dans un bécher de 250 m L puis on a ajouté 80 mL d'eau distillée.
Solution d'acide chlorydrique, notée Sa : C = 2,5.10^-2 mol.L
masse volumique du destop : p = 1,12 g.mL
Bonjour,
Tu as oublié de poster l'énoncé de l'exercice en entier.
Dans ce genre d'exercice je te conseille de faire un schéma simplifié du dispositif du dosage avec les données importantes de l'énoncé.
Sinon,
1. OK pour la méthode des tangentes et donc Ve = ?
2. Vues les bribes d'énoncé, ça semble OK.
Ces deux fiches vont ensuite t'aider à avancer :
![]() [lien]
[lien]
![]() [lien]
[lien]

Ce n'est pas un exercice mais un TP et je n'ai que ces informations pour répondre aux questions.
1) Ve = 100,5 mL
3) n(0)E = cD /vD
4) n(A)E = cA / vE
5) L'équivalence est le moment où les réactions ont été introduits dans les proportions stoechiométrique et entièrement consommés.
n(0)E/ 1 = n(A)E / 1
Bonjour,
Ce n'est pas un exercice mais un TP et je n'ai que ces informations pour répondre aux questions.
Si ton TP fait plusieurs pages, tu as le droit de nous fournir un pdf, passée la recopie des premières lignes :
 extrait de
extrait de Q05 - Puis-je insérer une image dans mon message ? Comment faire ? Quelle image est autorisée ?
Sinon, nous avons maintes fois travaillé ensemble sur des sujets, tu sais que la qualité rédactionnelle est primordiale dans un exercice scientifique.
Déjà, comme je te l'ai écrit dans mon message précédent, je te conseille de t'habituer à faire un schéma de principe :
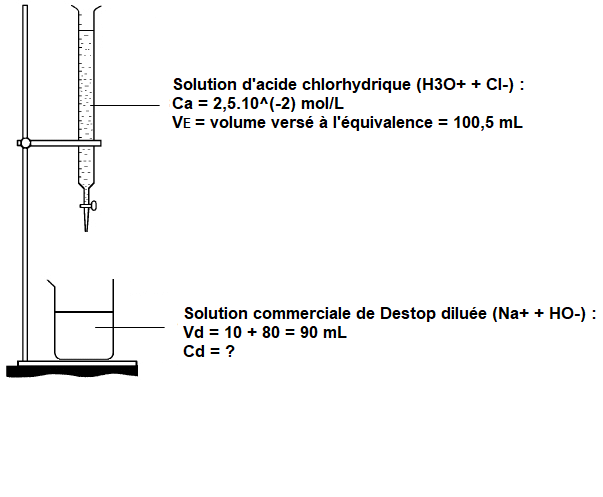
L'équation de la réaction du dosage est
L'équivalence est atteinte quand les réactifs de la réaction du dosage ont été introduits dans des proportions stoechiométriques.
Donc à l'équivalence,
La suite ?

c0 (solution commerciale) = cD * 100(facteur de dilution k)
c0 = 2,5.10^2 * 100 = 2,5 mol.L^-1 ?
Concentration massique :
s0 = m/V = n* M / V = C * V * M / V = C * M
s0 = C * M
= 2,5 * ( 23,0 + 16,0 + 1,0 ) = 100,0 g.mol^-1
C'est plus clair avec l'énoncé complet !
cD = cA * vE / vD
OK
cD = 2,5.10^-2 * 100,5.10^-3 / 90.10^-3 = 0,0279 mol/L = 2,8.10^-2 mol.L^-1
Effectivement, vues les données fournies, il vaut mieux mettre 2 chiffres significatifs au résultat.
c0 (solution commerciale) = cD * 100(facteur de dilution k)
c0 = 2,5.10^2 * 100 = 2,5 mol.L^-1 ?
Concentration massique :
s0 = m/V = n* M / V = C * V * M / V = C * M
s0 = C * M
= 2,5 * ( 23,0 + 16,0 + 1,0 ) = 100,0 g.mol^-1
Pas d'explication de ce que tu fais, pas de définition des notations utilisées => je ne lis pas !
A noter que je t'ai donné une fiche dans mon tout premier message pour poser un problème de dilution, ça peut aider pour la rédaction ...

Bonjour,
Le solution de Destop a été dilué 100 fois afin d'obtenir sD de concentration cD
Solution fille ( titrée, Destop diluée ) : vD = 90 mL et cD = ?
Solution mère ( titrante, acide chlorydrique ) : cA = 2,5.10^-2 mol.L^-1 et vE = 100,5 mL
Pour calculer c0, la solution commerciale Destop :
On utilise la relation qui lie les concentrations et le facteur de dilution :
F = c0 / C
c0 = F * cD
c0 = 100 * 2,8.10^-2 = 2,8 mol.L^-1
?
Concentration massique :
C0 = m/V = n* M / V = C * V * M / V = C * M
C0 = C * M
= 2,5 * ( 23,0 + 16,0 + 1,0 ) = 100,0 g.mol^-1
Pour la dernière question j'ai essayé de faire ceci :
m = n * M
or C = n / V donc n = C * V
Ainsi :
m = C * V * M(hydroxyde de sodium)
= 2,8.10^-2 * 100.10^-3 * ( 23,0 + 16,0 + 1,0 )
= 0,112 g = 0,1 g
mais pour 100 mL j'ai un peu de mal à le faire
Bonjour,
Le solution de Destop a été dilué 100 fois afin d'obtenir sD de concentration cD
Solution fille ( titrée, Destop diluée ) : vD = 90 mL et cD = ?
Solution mère ( titrante, acide chlorydrique ) : cA = 2,5.10^-2 mol.L^-1 et vE = 100,5 mL
Pour calculer c0, la solution commerciale Destop :
On utilise la relation qui lie les concentrations et le facteur de dilution :
F = c0 / C
c0 = F * cD
c0 = 100 * 2,8.10^-2 = 2,8 mol.L^-1
?
Houlà il faut que tu révises ce qu'est une dilution ! La solution mère et fille c'est du Destop plus ou moins dilué, pas un mélange d'acide chlohydrique et du Destop
Concentration massique :
C0 = m/V = n* M / V = C * V * M / V = C * M
C0 = C * M
= 2,5 * ( 23,0 + 16,0 + 1,0 ) = 100,0 g.mol^-1
Concentration massique de quoi ?
Pas clair
Je me suis perdue :
On utilise la relation qui lie les concentrations et le facteur de dilution :
F = c0 / C
c0 = F * cD
cD ( destop diluée )= 2,8.10^-2 mol.L^-1 d'après la question précédente.
c0 ( solution commerciale ) = 2,8.10^-2 * 100 = 2,8 mol.L-1 ??
Q8 :
C0 = m/V = n* M / V = C * V * M / V = C * M
C0 ( solution commerciale s0) = C0 * M
= 2,8 * ( 23,0 + 16,0 + 1,0 ) = 112,0 g.mol^-1 ???
Encore une fois, tu enchaînes l'utilisation de formules sans expliquer ce que tu fais.
Pose le problème comme dans la fiche car tu as deux dilutions à gérer : la première juste avant le titrage (ajout de 80 mL d'eau distillé) et celle initiale (solution diluée 100 fois).
1ère dilution :
solution mère : solution de Destop diluée 100 fois
V'd = 10,0 mL
C'd = ?
solution fille : solution de Destop diluée 100 fois avec ajout de 80 mL d'eau
Vd = 90 mL
Cd = 2,8.10-2 mol/L (déterminée grâce au titrage)
L'ajout d'eau ne modifie pas la quantité de matière donc V'd x C'd = Vd x Cd
<=> C'd = Cd x Vd / V'd
Deuxième dilution :
L'énoncé te donne une information précieuse : la solution commerciale a été diluée 100 fois, donc tu en déduis directement le facteur de dilution.
Ainsi : C'd = Co / 100 soit Co = C'd x 100
Ensuite, c'est une très mauvaise idée de l'énoncé d'utiliser la même notation pour la concentration molaire calculée et la concentration massique que je renomme Cmo.
Par définition de la concentration massique : Cmo = mo/Vo
si mo est la masse d'hydroxyde de sodium présente dans la solution de Destop et Vo son volume.
Et comme no = mo/Mo <=> mo = no x Mo, Mo étant la masse molaire de l'hydroxyde de sodium, alors :
Cmo = mo/Vo
Cmo = (no x Mo)/Vo
Cmo = no/Vo x Mo
Or par définition de la concentration molaire : Co = no/Vo si no est la quantité de matière en hydroxyde de sodium également présente dans cette solution.
Finalement Cmo = Co x Mo
Il ne reste plus qu'à exprimer la masse molaire en hydroxyde de sodium :
Mo = M(NaOH) = M(Na) + M(O) + M(H) = ... g/mol
C'd = Cd x Vd / V'd = 2,8.10^-2 * 90.10^-3 / 10,0.10^-3
= 2,52.10^-7 mol.L^-1
Co = C'd x 100 = 2,52.10^-7 * 100 = 2,52.10^-5 mol.L^-1
Mo = M(NaOH) = M(Na) + M(O) + M(H) = 40,0 g/mol
Cmo = Co x Mo = 2,52.10^-5 * 40,0 = 1,01.10^-3 mol.L-1 ?
Il y a une erreur dans tes calculs, tu ne peux pas trouver en résultat final une concentration d'une solution commerciale plus petite que celle de la solution diluée
Relis ton calcul ici :
C'd = Cd x Vd / V'd = 2,8.10^-2 * 90.10^-3 / 10,0.10^-3
= 2,52.10^-7 mol.L^-1
= 1
C'd = Cd x Vd / V'd = 2,8.10^-2 * 90.10^-3 / 10,0.10^-3
= 0,252 mol.L^-1 = 2,5.10^-2 mol.L^-1
Co = C'd x 100 = 2,5.10^-1 * 100 = 25 mol.L^-1
Mo = M(NaOH) = M(Na) + M(O) + M(H) = 40,0 g/mol
Cmo = Co x Mo = 25 * 40,0 = 1 000 mol.L-1
Il faut que tu aies un peu plus d'esprit critique sur les résultats que tu obtiens, ça te permettra de détecter les erreurs.
Déjà une concentration massique s'exprime en g/L et non pas mol/L.
Dans tous les cas, une solution de Destop d'1L qui contiendrait 1000 mol d'hydroxyde de sodium, cela reviendrait à vouloir dissoudre :
m(NaOH) = n(NaOH) x M(NaOH) = 1000 x 40,0 = 40 000 g = 40 kg dans 1 L d'eau !!!
Somme toute impossible ...
= 1
C'd = Cd x Vd / V'd = 2,8.10^-2 * 90.10^-3 / 10,0.10^-3
= 0,252 mol.L^-1 = 2,5.10^-2 mol.L^-1 => erreur commise
Co = C'd x 100 = 2,5.10^-1 * 100 = 25 mol.L^-1 à reprendre
Mo = M(NaOH) = M(Na) + M(O) + M(H) = 40,0 g/mol
Cmo = Co x Mo = 25 * 40,0 = 1 000 mol.L-1
C'd = Cd x Vd / V'd = 2,8.10^-2 * 90.10^-3 / 10,0.10^-3
= 0,252 mol.L^-1 = 2,5 mol.L^-1
Co = C'd x 100 = 2,5 * 100 = 250 mol.L^-1
Mo = M(NaOH) = M(Na) + M(O) + M(H) = 40,0 g/mol
Cmo = Co x Mo = 250 * 40,0 = 10 000 g.L-1 ???
C'est encore plus aberrant, pourtant j'utilise votre raisonnement d'hier
Il y a de nouveau une coquille :
C'd = Cd x Vd / V'd = 2,8.10^-2 * 90.10^-3 / 10,0.10^-3
= 0,252 mol.L^-1 = 2,5.10-1 mol.L^-1
Co = C'd x 100 = 2,5.10-1 * 100 = 25 mol.L^-1
Mo = M(NaOH) = M(Na) + M(O) + M(H) = 40,0 g/mol
Cmo = Co x Mo = 25 * 40,0 = 1000 g.L-1
Pour une solution commerciale à 10%, cela revient à dire qu'il y a 10g de NaOH dissout pour 100 g de solution (environ 89 mL de solution).
10 g <=> 89 mL
x g <=> 1000 mL
soit x = 112g de NaOH par litre de Destop
Il y a donc effectivement un souci quelque part :
- soit ça vient du volume versé à l'équivalence qui est élevé par rapport à la solution diluée de Destop titrée ;
- soit l'énoncé considère qu'on ne doit pas tenir compte des 80 mL d'eau distillée versés dans le bécher avec les 10 mL de la solution de Destop diluée 100 fois mais ça serait saugrenu
Je ne comprends pas l'erreur que j'ai commis ( 10^-1) donc je ne vais pas arrondir :
C'd = Cd x Vd / V'd = 2,8.10^-2 * 90.10^-3 / 10,0.10^-3
= 0,252 mol.L^-1
Co = C'd x 100 = 2,5 * 100 = 25,2 mol.L^-1
Mo = M(NaOH) = M(Na) + M(O) + M(H) = 40,0 g/mol
Cmo = Co x Mo = 25,2 * 40,0 = 1 008 g.L-1 ???
Tu es quand même d'accord que 0,252 mol/L = 2,52.10-1 mol/L ?
Qu'il est préférable de réduire à 2 chiffres significatifs : 2,5.10-1 mol/L.
Dans tous les cas, avec 2 ou 3 chiffres significatifs, ça ne changera pas le constat final





