Inscription / Connexion Nouveau Sujet
Diagramme changement d'état MnO-Al2O3
Bonjour à tous je vous explique mon problème je dois repérer les points particulier du diagramme de changement d'états de MnO-Al2O3 (que j'ai joint) ou dire des choses que l'on peut en déduire grâce à celui-ci pour en faire la présentation lors d'un oral (Le sujet c'est "MnAl2O4 as a magnetic material") .
Sauf que je ne trouve pas grand chose à dire à part que :
- pour faire la synthèse de MnAl2O4 il est nécessaire de partir de ce diagramme de changement d'état car pour en faire la synthèse il nous faut une fraction très précise de MnO et de Al2O3
Sinon je n'arrive pas trop à repérer les points caractéristique du diagramme...
Je demande donc votre aide à ce sujet en essayant de m'expliquer pourquoi telle ou telle chose serait intéressante à dire à l'oral.
Merci beaucoup !
Bonsoir totob85,
Face à ce genre de diagramme, il est en général bon de:
- identifier les phases dans chacune des zones. Et vue le sujet "MnAl2O4 as a magnetic material", discuter des propriétés magnétiques des différentes phases (il te faudra faire des recherches internet pour ce dernier point).
- identifier les points singuliers (corps purs, eutectique, etc.). Et discuter l'intérêt de ces points. Es-tu à l'aise avec ce genre de diagramme ?
- identifier la nature de la transformation à chaque interface (fusion/solidification, changement de phase sans changement d'état, etc.). Et discuter les changements de pente (ex: horizontal = à température constante).
Bon courage,
Metal Oxalate
Bonjour MetalOxalate et merci de votre réponse.
Il est vrai que je ne suis pas très a l'aise avec ces diagrammes cependant je pense avoir repéré un palier eutectique et un palier péritectique je vous joint une illustration pour que vous soyez en accord avec moi.
Dailleur peritectique et eutectique qu'est ce que cela implique ? il me semble que c'est en dessus des ces paliers la composition devient "spéciale" non ? pourriez-vous m'en dire un peu plus ?
de plus j'aimerais essayer de repérer les points où le composer est à l'état solide, liquide ou même gazeux même si je ne crois pas qu'il passe à l'état gazeux. Car je n'arrives pas a distinguer cela. ( je vous joint aussi une ébauche de ma part concernant ce sujet pour que vous puissiez confirmé oubien m'indiquer d'autres infos supplémentaires.
Bon, c'est déjà pas mal  . Je vois que tu as un peu dépatouillé le sujet.
. Je vois que tu as un peu dépatouillé le sujet.
Concernant les notions d'eutectique et péritectique:
Un eutectique est un mélange qui fond (ou se solidifie) à température constante et de manière uniforme. Il existe alors un point où les courbes solidus et le liquidus se touchent.
- les coordonnées de E donnent sa composition et son point de fusion.
- le point de fusion de E est inférieur au point de fusion des composants pris séparément.
remarque: la phase liquide est en équilibre avec 2 solutions solides
Un peritectique est un mélange dont la fusion conduit à la formation d'un liquide et un nouveau solide (phase différente).
remarque: il ne suffit pas de refroidir un mélange liquide dont la composition correspond au péritectique pour l'obtenir. On parle alors de fusion non-congruente.
remarque: la phase solide est en équilibre avec 1 liquide et 1 autre solide.
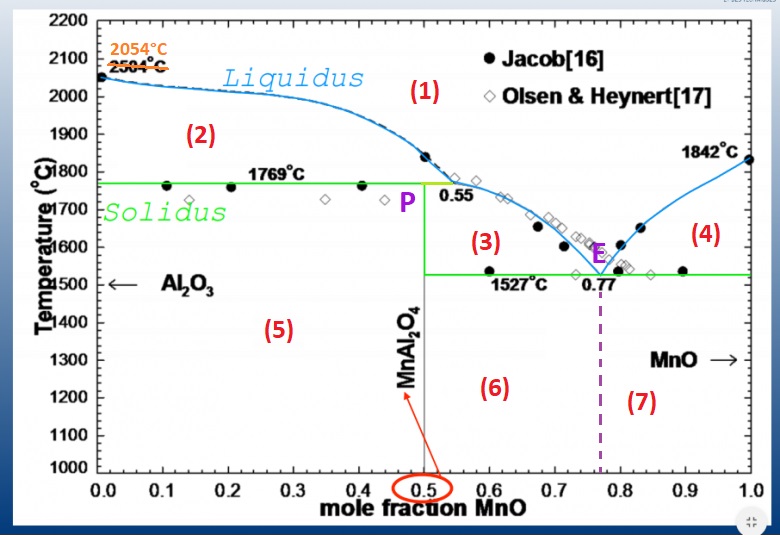
J'ai retouché ton diagamme, pour y faire apparaitre 7 zones ainsi que (E) et (P).
Je te propose à présent d'identifier les espèces et leur état physique (solide et/ou liquide)  .
.
- zone 1: Au dessus du liquidus, donc que du liquide (rien de plus à dire)
- zone 2: Sous le liquidus, mais au-dessus du solidus. On a donc un liquide et un solide (reste à identifier les espèces).
- zone 3: Sous le liquidus, mais au-dessus du solidus. On a donc un liquide et un solide. On est à gauche de l'eutectique et à droite du péritectique (reste à identifier les espèces)
- zone 4: Sous le liquidus, mais au-dessus du solidus. On a donc un liquide et un solide. On est à droite de l'eutectique (reste à identifier les espèces)
- zone 5: sous le niveau péritectique, à gauche de la droite péritectique. Solution solide de 2 espèces (lesquelles?)
- zone 6: sous le niveau eutectique, à gauche de l'eutectique (zone hypo-eutectique) mais à droite du péritectique. Solution solide de 2 espèces (lesquelles?)
- Zone 7: sous le niveau eutectique, à droite de l'eutectique (zone hyper-eutectique). Solution solide de 2 espèces: (E) + MnO, tout deux solides.
A l'aide de l'exemple de la zone 7, vois-tu comment faire pour les autres zones?
Bonne chance 
J'ai retouché ton diagamme, pour y faire apparaitre 7 zones ainsi que (E) et (P).
Je te propose à présent d'identifier les espèces et leur état physique (solide et/ou liquide)
 .
.
- zone 1: Au dessus du liquidus, donc que du liquide (rien de plus à dire)
- zone 2: Sous le liquidus, mais au-dessus du solidus. On a donc un liquide et un solide (reste à identifier les espèces).
- zone 3: Sous le liquidus, mais au-dessus du solidus. On a donc un liquide et un solide. On est à gauche de l'eutectique et à droite du péritectique (reste à identifier les espèces)
- zone 4: Sous le liquidus, mais au-dessus du solidus. On a donc un liquide et un solide. On est à droite de l'eutectique (reste à identifier les espèces)
- zone 5: sous le niveau péritectique, à gauche de la droite péritectique. Solution solide de 2 espèces (lesquelles?)
- zone 6: sous le niveau eutectique, à gauche de l'eutectique (zone hypo-eutectique) mais à droite du péritectique. Solution solide de 2 espèces (lesquelles?)
- Zone 7: sous le niveau eutectique, à droite de l'eutectique (zone hyper-eutectique). Solution solide de 2 espèces: (E) + MnO, tout deux solides.
A l'aide de l'exemple de la zone 7, vois-tu comment faire pour les autres zones?
Bonne chance


Rebonjour MetalOxalate !
Merci de votre implication sur le sujet c'est très gentil, désolé de répondre si tard j'étais assez occupé.
Je me suis penché sur vos questions des zone de 1 à 7 et voici ce que je pense :
1: Tout liquide
2: Al2O3 + liq
3: MnAl2O4+ liq
4: MnO + Liq
5: Al2O3 + Mnal2O4
6: MnAl2O4+ MnO
7: idem
Encore merci !

Oui, très bien, c'est ça  .
.
Petite différence entre la zone 6 et 7: même espèces en présence mais différente proportion.
Zone 6: MnAl2O4 majoritaire, MnO minoritaire
Zone 7: MnO majoritaire, MnAl2O4 minoritaire
Ton sujet d'exposé portant sur MnAl2O4 et ses propriétés magnétiques, on va s'intéresser à sa synthèse, identifier quelques aspects de production (quantités de matière première par kg de MnAl2O4 ; température de chauffe; pureté de produit), ainsi que quelques pistes d'optimisation (pureté et qualité de produit VS coût de production et impact environnementaux).
1- Production à partir d'un mélange de composition péritectique
- quelle sont les coordonnées péritectique (%mol; Temp)?
- Si on part d'un mélange liquide dont la composition correspond au péritectique, que forme-t-on à 1,500°C (et dans quelle proportion)?
- même question, si on refroidit jusqu'à 1,200°C (et dans quelle proportion)?
2- Production de MnAl2O4 pur
- Quelle composition initiale de liquide (en %mol) permet théoriquement de produire MnAl2O4 pur?
- En deduire les quantités (en kg) de MnO et Al2O3 (supposé pur) nécessaires pour produire 1 kg de MnAl2O4
3- Cout de production et impact environnemental
Une part importante des couts de production en métallurgie est due à la puissance de chauffe (T ~2,000 °C!).
Ce chauffage est aussi la cause d'impact environnementaux (CO2 émis pour produire la chaleur dans les hauts fourneaux ou électricité nécessaire pour former un arc électrique, consommation d'eau de refroidissement, etc.). Là encore, si on voit qu'il y a un intérêt à faire baisser la température de fonctionnement 
La courbe du liquidus montre que la température de fusion varie de 2057°C (Al2O3 pur) à 1527°C (Eutectique), en fonction de la composition initiale.
- Si on souhaite faire baisser les prix et notre impact environnemental, vaut-il mieux se placer à gauche ou à droite de la composition déterminée en "2- Production de MnAl2O4 pur"?
- Si on s'autorise un décalage de 0.04 points sur la composition initiale du mélange, de combien baisse la température de fusion? Quel sera la pureté (en %mol et %mass) du produit MnAl2O3? commenter. Dans la suite on appelera cette composition éco-MnAl2O4.
- Si on s'autorise un décalage de 0.2 points sur la composition initiale du mélange, de combien baisse la température de fusion? Quel sera la pureté (en %mol et %mass) du produit MnAl2O3? commenter. Dans la suite on appellera cette composition super éco-MnAl2O4.
4- Propriétés magnétiques du produit
- Quelles sont les propriétés magnétiques de MnO, Al2O3 et MnAl2O4?
- Discuter de l'impact (ou non-impact) d'impureté (MnO, Al2O3) dans le produit (MnAl2O4).
- Conclure quant à l'éventuelle acceptabilité (qualité produit) d'un bloc de super-éco, puis d'éco-MnAl2O4 comparé à un bloc de MnAl2O4 pur.
NB: il ne s'agit que d'une suggestion de questions et de réflexions à aborder dans ta présentation. Libre à toi d'étudier d'autres questions  .
.
Si une application précise du MnAl2O4 est déjà envisagée, ça peut être bien d'en parler et faire le lien (si possible) avec le diagramme de phase  .
.
Bon courage,
Metal Oxalate


