Inscription / Connexion Nouveau Sujet
Calcul d'un potentiel standard inconnu
Bonjour j'ai un exercice assez classique en oxydoréduction en solution aqueuse ou on a deux demi piles.
D'un coté on a une cathode constitué d'une électrode de Fer dans une solution de Fe2+ et d'un autre une électrode M de métal inconnue plongée dans une solution de M(NO3) de concentration 1 mol/L
On nous dis qu'on mesure la fem de la pile: fem=1,24v
On laisse la pile fonctionner pendant une nuit et on voit que 'electrode de fer s'est allégé et que l'autre s'est alourdi.
On nous donne aussi le potentiel standard du couple Fe/Fe2+=-0,44V
J'ai traité toutes les questions de l'exo
Cependant j'ai un doute quand on me demande le potentiel standard du couple M+(aq)/M(s)
Est ce qu'il faut juste faire E° cathode= Fem + E° anode soit 0,8V ou c'est plus compliqué?
Merci d'avance pour l'aide.
Bonjour lunlub,
Depuis le temps que tu es sur le forum, tu sais qu'il faut fournir un énoncé complet qui servira de base pour tes échanges mais aussi pour les futurs membres qui seraient intéressés par ton exercice pour s'entraîner.

Ok donc on a connecté les deux demi piles à 25°C avec un voltmètre pour calculer la fem de la pile fem=1,24v
(C'est tout ce qu'il y a de plus dans l'énoncé)
Q1) Ecrire les équations aux électrodes puis l'équation de fonctionnement de la pile
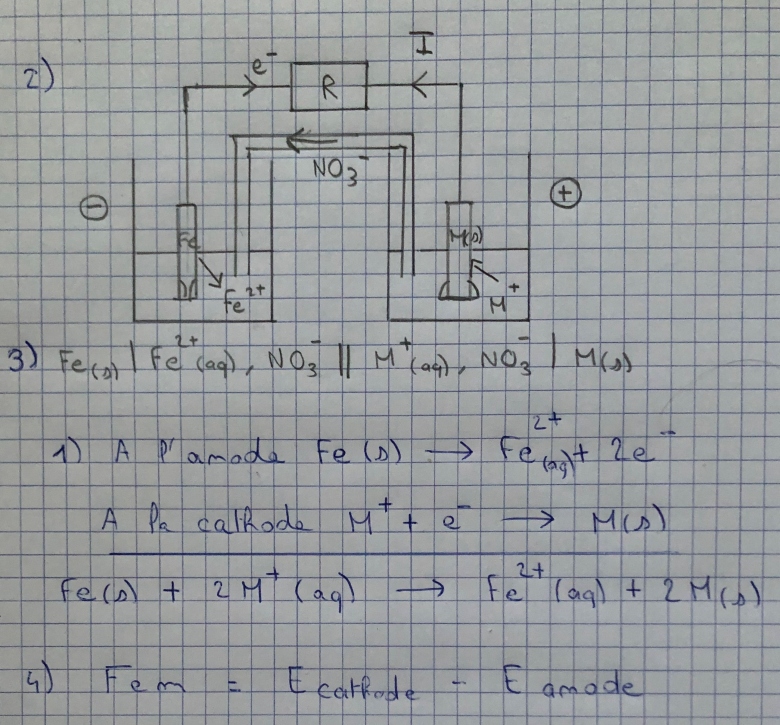
Q2) Compléter le schéma donné en donnant le sens du courant, des électrons et des ions
Q3) Donner l'écriture conventionnel de la pile.
Q4) Quelle est le potentiel standard du couple M+(aq)/M(s)?
Je peux poster une photo du schéma gbm?
Bonjour
L'énoncé précise-t-il quel est le pôle + de la pile ? La concentration en ions fer(II) est-elle précisée ?
Dans le cas général, la fém est la différence entre les potentiels de Nernst des deux demies piles. Il s'agit de la différence entre les deux potentiels standard que si les deux demies piles fonctionnent dans les conditions standard...
Vanoise -> L'énoncé n'indique pas le pôle de la pîle ni la concentration en ions fer(II)
Il est par contre effectivement indiqué que la demi pile Fe2+/Fe est une demi pile standard. Ce n'est pas indiqué pour la demi pile de métal inconnue.
Du coup c'est bon d'après toi?
Ok vanoise tu as raison c'est dans les conditions standard et il est effectivement indiqué que l'on est à T=25°C
En supposant : [Fe2+] = [M+] = 1mol/L , les deux demies piles sont effectivement dans les conditions standard.
En supposant que la demie pile correspondant au couple M+/M est bien la cathode, ton raisonnement est correct.
Quelques remarques : les deux solutions sont électriquement neutre : elles contiennent toutes deux des ions négatifs (ions nitrate par exemple)
Le pont salin est très souvent une solution de chlorure de potassium. Le courant y est assuré par un double déplacement d'ions : ions K+ dans le sens conventionnel du courant et ions Cl- en sens inverse.