Inscription / Connexion Nouveau Sujet
Vitesse de transformations spontanées en électrochimie
Bonsoir, comment dois-je raisonner pour savoir si les 4 transformations suivantes sont spontanées ou non ? De plus, comment argumenter sur leur vitesse ? C'est vraiment le raisonnement, la méthode qui m'importent le plus.
(Je vois ça actuellement en 2èmeannée de prépa.)
Merci d'avance à toute personne m'accordant un peu de son temps.
Bonjour,
Pour qu'une demi réaction ait lieu de manière appréciable, il faut que le courant (image de la vitesse) ait une valeur sensible. Il s'agit donc de trouver l'intensité de ce courant.
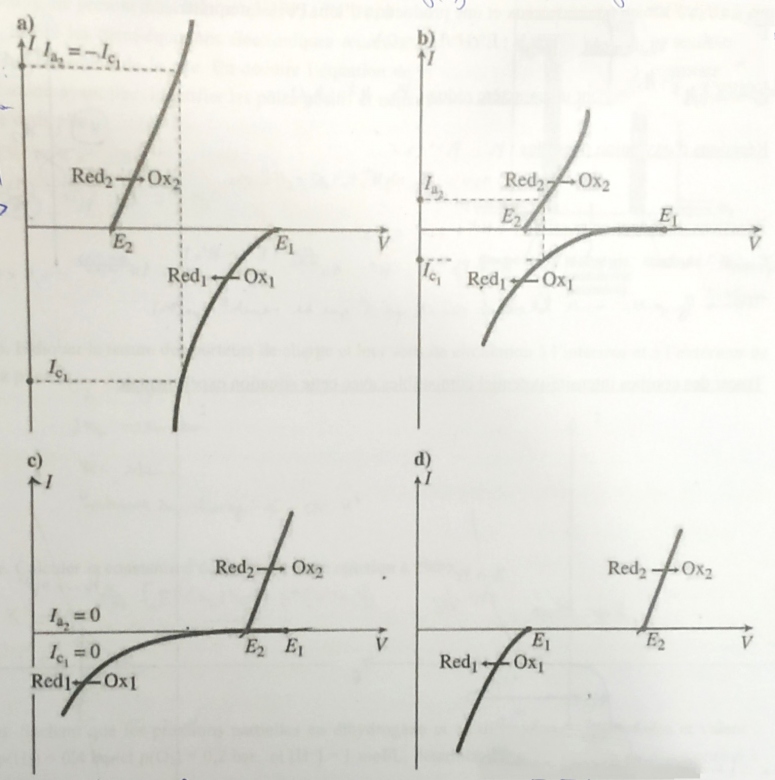
Comme on a deux couples dans la même solution, on a deux conditions à respecter : égalité des potentiels et égalité des vitesses (donc courant opposés) : c'est déjà dessiné sur les deux premiers graphes.
Sur les deux autres, on voit que lorsque la condition est respectée, le courant est quasi nul.
Bonjour,
Pour qu'une demi réaction ait lieu de manière appréciable, il faut que le courant (image de la vitesse) ait une valeur sensible. Il s'agit donc de trouver l'intensité de ce courant.
Comme on a deux couples dans la même solution, on a deux conditions à respecter : égalité des potentiels et égalité des vitesses (donc courant opposés) : c'est déjà dessiné sur les deux premiers graphes.
Sur les deux autres, on voit que lorsque la condition est respectée, le courant est quasi nul.
Merci beaucoup pour votre réponse. Y a-t-il une explication qui me permettrait de comprendre les 2 conditions nécessaires que vous avez donné ?
Pour ce qui est des courants l'explication a été donnée.
Pour ce qui est des tensions, imaginez une électrode fictive isolée qui plonge dans la solution, cette électrode a une tension et une seule et c'est le V de votre axe.
L'électrode fictive est bien sûr réelle lorsqu'on trace séparément les deux courbes i-E.


