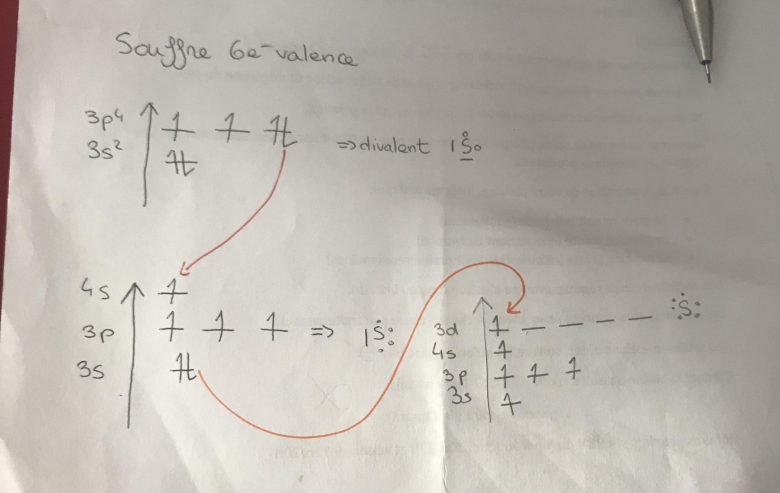Inscription / Connexion Nouveau Sujet
Valence du souffre
Bonjours, j'essaie de retrouver les différentes valences du souffre grâce à la configuration fondamentale.
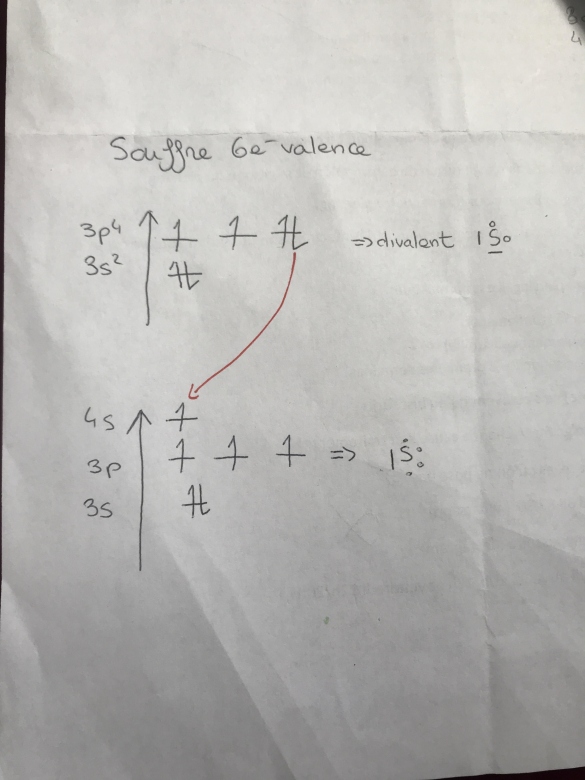
Pour la divalence il n'y a pas de soucis.
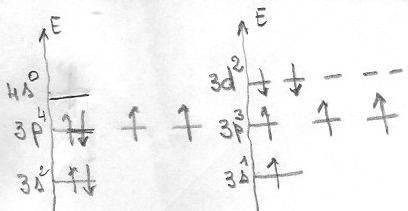
Pour les 4 liaisons et le doublet non liants j'ai lu qu'il y a avait promotion d'un électron de la sous-couche 3p sur la 4s.
Cependant je ne comprends pas quelle est la configuration lorsque le souffre fais 6 liaisons. Quels électrons sont promus sur des couches supérieures et lesquelles ?
Merci de votre aide
Remarque préalable : l'élément qui nous occupe n'a rien à voir avec le verbe souffrir ; il s'agit de l'élément soufre écrit avec un seul "f".
Sinon, tu as sans doute vu en cours que les écarts d'énergies entre les différents niveaux se réduisent au fur et à mesure que la valeur du nombre quantique principal "n" augmente. Les niveaux 3d et 4s sont extrêmement proche. Compte tenu de la géométrie des molécules telles que SF6 (voir message précédent), il faut envisager lors de la formation de la molécule, une excitation (apport d'énergie) de deux électrons au niveau 3d conformément au schéma ci-dessous.