Inscription / Connexion Nouveau Sujet
Usure d'une pile
Bonjour,voici un petit exercice de niveau 3ème. Je bloque sur la 3ème question. Merci d'avance pour toute aide.
Un matin, Anaelle réalise une pile avec une solution de sulfate de cuivre, une lame de cuivre et une lame de zinc.
Elle branche la pile n série avec un ampèremètre et un conducteur ohmique. Elle dresse un tableau dans lequel elle
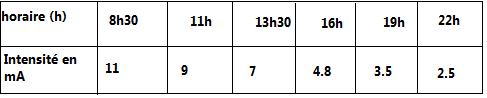
note l'heure du relevé et l'intensité du courant. Elle obtient le tableau-ci dessous.
1)Que peut observer Anaelle au niveau de la lame de zinc ?
2)Quel est l'aspect initial de la solution ? Comment évolue-t-il ?
3)Le lendemain Anaelle ajoute un peu de sulfate de cuivre en poudre dans la solution. Que peut elle constater ?
Ta pile contient 3 élements
2lames une de cuivre et une de zinc et une solution de sulfate de zinc
La concentration en ion zinc du sulfate de zinc est assez faible, alors que la quantité de cuivre et de zinc est nettement supèrieure à celle du sulfate de zinc
Pendant la réaction les ions Zn2+ réagissent pour devenir du zinc, la concentration diminue donc et l'intensité de la pile diminue
Si tu en rajoutes la concentration augmente et donc.....


