Inscription / Connexion Nouveau Sujet
Une solution de sulfate de cuivre
Bonjour !! 
J'ai un exercice et je voudrais votre correction mais aussi votre aide pour 2 questions ...
Enoncé: Le spectre d'absorption d'une solution aqueuse de sulfate de cuivre est donné ci dessous. (voir image)
A quelle longueur d'onde lambda max faut'il se placer pour effectuer avec précisions les mesures d'absorbance ? Justifier!
Ma réponse: il faut se placer à lambda max=800. (car il faut se placer à la longueur d'onde correspondant au max d'absorption.
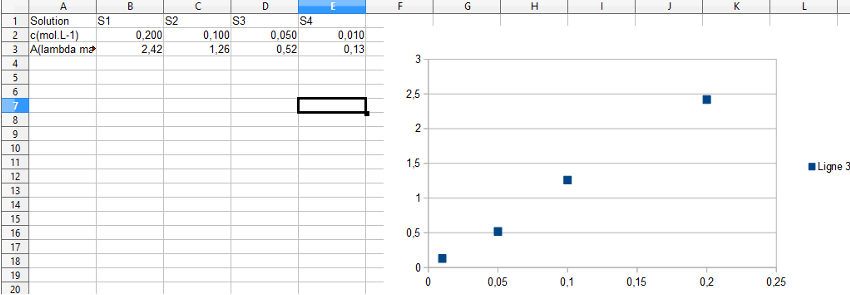
2) On prépare 4 solutions aqueuses de sulfate de cuivre dont les concentrations molaire c en soluté apporté et les valeurs d'absorbance A et lambda max sont données ci dessous. (voir tableur)
a)Tracer le graphe représentant l'absorbance en fonction de la concentration molaire (voir tableur) (je n'ai pas encore mis le titre et les unités mais je vais le faire)
Petite question en + : comment je peux renommer le "ligne 3" ?
b) Quelle est la nature de la courbe obtenue ?
Ma réponse: C'est une droite qui passent par l'origine et qui relit quasiment tout les points corespondants aux solutions qui sont presques alignés.
c)Quelle loi est ainsi mise en évidence ? Justifier !
Ma réponse: La courbe met en relation l'absorbance à la concentration des solutions de plus elle passe par l'origine donc l'absorbance est proportionnelle à la concentration des solutions . C'est donc la loi de Beer Lambert.
d)Déterminer la relation numérique entre A et c
Ma réponse: K est un coeff de proportionnalité
L'équation de la droite est donc de A800= K*c
K est aussi le coeff directeur de la droite.
Pour trouver K je prends 2 points A' et A'' (sur la droite)
A'(0;0) A''(2.42;0.200)
K=(A''800- A'800)/(c''-c)
K=(2.42-0)/(0.200-0)
K= 12.1 mol.L-1
La relation numérique est 12.1*c
e)Le coefficient trouvé sera t'il supérieur ou inférieur si l'on réalise les mêmes mesures à la longueur d'onde 650 nm ?
A cette question je suis bloqué car je ne sais pas par ou commencer ...
Merci pour votre aide et désolé pour les photos ... je ne sais pas vraiment si j'ai le droite de les mettre ...
Merci d'avance !
bonjour,
tes réponses sont correctes.
en a),la ligne 3 peut-être renommée "absorbance"
d) l'unité de K es L.mol-1 puisque l'absorbance est sans unité
e) on a A=k*C
tu as écris :
Ma réponse: il faut se placer à lambda max=800. (car il faut se placer à la longueur d'onde correspondant au max d'absorption.
Conséquence :si on choisit une autre valeur pour
 ,que devient A?
,que devient A?
Donc que devient k ?
Merci !
Est ce que pour la d) je dois faire tout mon calcul ou est ce que je peut simplement ecrire que la relation numérique est A= K*c
Pour la e) comme 650 nm< 800 nm
K de 650 nm < K de 800 nm
Donc coefficient inférieur
bonsoir ,
Ce n'est pas parce que 650nm <800 nm que K(650)<K(800) mais parce que à 650nm l'absorbance est plus faible qu'à 800 nm.
(Ce serai aussi vrai à 900nm.)
En résumé:
pour une concentration donnée,l'absorbance est plus faible à 650 nm qu'à 800nm.
Puisque A est proportionnel à K, si A diminue,K diminue
Bonsoir,
J'ai une question par rapport à la question 2)d. Vous avez trouvé K = 12,1 L. mol-1 en utilisant les valeurs de S1 (c'est-à-dire c=0,200 et A=2,42). Mais j'ai utilisé les valeurs de S4 et j'ai trouvé K = 0,13/0,010=13 L. mol-1.
Est-ce que c'est normal de trouver des valeurs de K différentes ?
Merci pour votre aide.
Bonjour à tous.
A Erinye...
Est-ce que c'est normal de trouver des valeurs de K différentes ?
Les points de la courbe sont sensiblement (mais pas parfaitement) alignés et la droite obtenue passe par l'origine ; l'équation de la droite sera donc de type A = K C.
En choisissant l'un ou l'autre des points de la droite tracée, on peut trouver des valeurs du coefficient directeur légèrement différentes.
Généralement, dans ce type de situation, on trace une droite passant par le maximum de points expérimentaux (ainsi que par l'origine du repère) et on utilise pour le calcul du coefficient directeur un des points effectivement situés sur la droite qui a été tracée.
On peut aussi, si on utilise un tableur, demander au logiciel de tracer la" droite de régression" (càd la droite lissée) et d'afficher l'équation de cette droite.
Il suffit pour cela de sélectionner la courbe qui a été tracée, de faire un clic droit et de choisir les options convenables dans la boîte de dialogue qui s'ouvre alors.
A plus.


