Inscription / Connexion Nouveau Sujet
TP Synthèse de la p-methyl benzophenone
Bonsoir,
J'ai deux petites questions dans mon TP dont je ne parviens pas a résoudre.
a) Quelles réactions autres que l'acylation peuvent-être faites par substitution électrophile catalysée par un acide de Lewis sur un composé aromatique ?
b) Peut-on préparer par la réaction de Friedel et Crafts la butan-2-one ?
Bonjour ,
1) Par substitution électrophile tu peux réaliser des halogénations en utilisant par exemple Br2 en présence d'un catalyseur comme FeBr3 ou AlBr3. Tu peux aussi réaliser des alkylations
2) Il n'y a pas d'aromatique dans le butan-2-one, donc je ne vois comment préparer cette molécule par Friedel et Crafts
Bonjour,
Je ne parviens pas à résoudre ces questions.
Le but de la manipulation est de préparer la p-méthylbenzophénone par la réaction du chlorure sur le toluène en excès qui servira de solvant
a) Quelle est la nature du chlorure de benzoyle ? Pourquoi dit-on que le composé intermédiaire formé est un électrophile ?
b) Après la réaction le chlorure d'aluminium n'est pas libérer, mais forme un complexe avec la cétone préparer. Quelle peut-être la nature de ce complexe ? Conclure quant à la quantité de chlorure d'aluminium à utiliser.
*** message déplacé ***
Bonjour à vous deux,
@laurinep : poster par bribes son TP dans plusieurs sujets est strictement interdit (1 sujet créé = 1 exercice = 1 TP ...) 
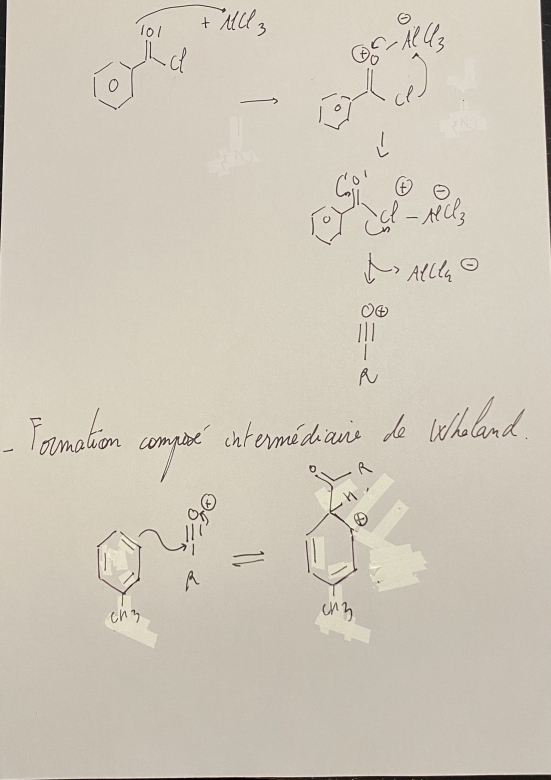
Je t'ai dessiné le mécanisme de la réaction pour l'explication soit plus claire. Donc AlCl3 qui est utilisé comme catalyseur sert a activé ton organochloré. Et ensuite ton toluène vient réagir avec ton agent acylant. Et tu vois bien que l'intermédiaire que tu formes lors de la réaction possède une charge +, cette intermédiaire de Wheland est donc électrophile.
À la fin tu finis par régénérer ton AlCl3, mais ce dernier est un acide de lewis, c'est-à-dire qu'il possède une lacune.
Et donc ta cétone formée va venir l'attaqué pour former un complexe. Et donc tu vois bien que AlCl3 ne peut pas être utilisé pour reformer une autre cétone car il est engagé dans un complexe. Il faut donc utiliser un peu plus de 1 équivalent par rapport au chlorure de benzyle. On en met un peu plus de 1 pour être sûr que tout réagisse.