Inscription / Connexion Nouveau Sujet
TP - pH-métrie et dosage de polyacides
Bonsoir,
Je travaille actuellement sur la partie théorique d'un TP de pH-métrie et j'aurais quelques questions.
On considère la neutralisation de l'acide phosphorique. On me demande d'exprimer le taux de dissociation α d'une solution de H3PO4 de concentration Ca en fonction de Ka1 et de Ca.
1) Dans un premier temps, j'ai considéré la réaction : HA + H2O = A- + H3O+
Mais après avoir relu l'énoncé, cette équation ne semble pas correspondre à une neutralisation (si j'ai bien compris, il s'agit de faire réagir l'acide avec une base pour former de l'eau et un sel)...
J'aurais pu m'arrêter là en réécrivant la bonne équation, mais le problème est que mon résultat (voir l'expression de α1 à la fin du message) correspond à une formule vue en cours. Cette formule est-elle malgré tout adaptée à la situation ?
2) Dans un second temps, j'ai considéré la réaction de neutralisation HA + HO- = A- + H2O, que je considère comme étant celle attendue.
Si cette réaction est la bonne, elle me poserait problème au niveau du tableau d'avancement. Comment remplir le tableau d'avancement avec Ca et α ?
Vous l'avez constaté, je me suis complètement embrouillé... Qu'est-il réellement attendu et quelles sont les étapes pour y parvenir ? Merci d'avance pour vos réponses !
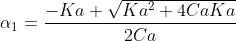
Bonjour
Pour étudier le taux initial de réaction sur l'eau, il faut effectivement utiliser la première équation.
En 2 : ton équation de réaction de titrage est correcte mais attention, l'acide phosphorique est un triacide. Il serait donc préférable de le noter H3A.
Le cas du titrage de l'acide phosphorique est un des plus délicat compte tenu des valeurs des pKa... As-tu bien compris au préalable le titrage d'un monoacide faible ?
J'ai déjà eu l'occasion de traiter ce titrage dans le cas Ca=10-2mol/L. C'est un peu plus simple pour Ca=0,1mol/L...
![]()
Cela va peut-être te paraître assez compliqué... Tu as peut-être intérêt à étudier ce cas plus simple d'abord :
![]()
Merci pour vos réponses et vos précisions, j'ai bien consulté les 2 liens que vous m'avez fourni.
Donc quand on nous demande le taux de dissociation, il s'agit toujours du taux de dissociation dans l'eau ?
Je pense avoir compris le titrage d'un monoacide faible (avec le cas de l'acide éthanoïque réalisé la semaine dernière).
Dans la suite du TP, on nous demande justement de traiter les cas Ca = 10-2 mol/L et Ca = 10-1 mol/L et d'en déduire la réaction prépondérante entre l'acide phosphorique et la soude (pour chaque valeur de Ca).
- Pour Ca = 10-2 mol/L, je trouve α = 62%
- Pour Ca = 10-1 mol/L, je trouve α = 27%
J'ai compris les grandes lignes de la réaction prépondérante, mais ma maîtrise est encore fragile. Sachant qu'on a trouvé le taux de dissociation de l'acide dans l'eau, quel est le lien à faire avec le réaction prépondérante entre l'acide et la soude ?
Le calcul du taux de dissociation avant titrage est mené au paragraphe 3.1 du premier document. Pour Ca=10-2mol/L j'obtiens h/Ca=55,5% mais la valeur de Ka fournie par ton professeur est peut-être un peu différente de celle que j'ai retenue. Même méthode pour Ca=0,1mol/L.
Sachant qu'on a trouvé le taux de dissociation de l'acide dans l'eau, quel est le lien à faire avec le réaction prépondérante entre l'acide et la soude ?
Voir paragraphe 2 pour les réactions prépondérantes. Le raisonnement ne porte pas sur les taux de réaction mais sur le fait que la constante d'équilibre est( ou n'est pas) très grande devant "1".
Effectivement, on nous donne un pKa de 2,0 pour le couple (H3PO4/H2PO4-) au lieu des 2,16 utilisés dans votre document, d'où mon résultat. Avec la même méthode, je retrouve bien les résultats obtenus précédemment pour les deux concentrations.
Merci pour cette précision concernant ce qu'on attend de nous avec les réactions prépondérantes. J'avais bien lu ce paragraphe : mon souci concerne la méthodologie et la compréhension globale de ce qu'on attend de nous.
On nous dit de trouver la réaction prépondérante entre l'acide phosphorique et la soude : selon mon idée, en utilisant la "règle du gamma" que vous évoquez, je trouve que :
H3PO4 + HO- = H2O + H2PO4-
Cela correspond à ce que vous avez indiqué pour Ca = 10-2 mol/L (j'obtiens un K = 1012 >> 1)
Concernant Ca = 10-1 mol/L : Je n'arrive pas à visualiser le fait que la réaction prépondérante entre l'acide phosphorique et la soude puisse être différente selon la concentration Ca... Je serais tenté de dire que cette réaction prépondérante est la même pour les deux concentrations. Mais je me doute que si on nous pose la question, c'est que ce n'est sûrement pas le cas.
Je n'arrive pas à visualiser le fait que la réaction prépondérante entre l'acide phosphorique et la soude puisse être différente selon la concentration Ca
Tu ne m'as pas bien compris. Le taux de réaction sur l'eau avant début du titrage dépend de Ka et de Ca. En revanche, le fait qu'une réaction puisse être considérée comme quasi totale ou non dépend seulement des constantes d'équilibre. Classer comme je l'ai fait en haut de la page 2 les différents couples en fonction de leur pKa, aide grandement à la détection des réactions prépondérantes. Le tracé des domaines de prédominances ($1) aide beaucoup à la compréhension et permet parfois d'un simple coup d'il de vérifier la cohérence des résultats.
Mon problème est surtout ici : "En déduire la réaction prépondérante entre l'acide phosphorique et la soude pour chaque concentration."
On nous donne pKa(H3PO4/H2PO4-) = 2,0. Pour répondre à la question, j'ai du mal à voir ce qui va changer dans les constantes d'équilibre pour chaque concentration Ca (10-2 mol/L et 10-1 mol/L). J'ai bien compris ceci :
Le fait qu'une réaction puisse être considérée comme quasi totale ou non dépend seulement des constantes d'équilibre
Il faudrait exprimer K en fonction de Ka et Ke, mais le Ka ne reste-t-il pas fixe vis-à-vis des conditions initiales (donc égal à 2 en permanence si la température ne varie pas) ? Je ne vois pas comment résoudre le problème pour chacune des concentrations, car je ne visualise pas ce qui changerait (selon mon idée, on retrouverait strictement les mêmes K pour 10-1 et 10-2 mol/L). Je ne sais donc pas ce que l'on attend de nous "pour chaque concentration".
Je précise que, dans mon cours, il est indiqué que lorsque la constante d'équilibre est supérieure à 103, on la considère comme totale et on recommence la méthode de la réaction prépondérante jusqu'à obtenir un équilibre.
Merci d'avance pour les clarifications que vous pourrez m'apporter,
Bonne journée.
Toute l'expérience est supposée se dérouler à la température fixe de 25°C, ce qui permet de considérer les diverses constantes d'équilibre fixes et égales aux valeurs fournies par les tables thermodynamiques.
Que l'on ait Ca=0,01mol/L ou Ca=0,1mol/L, le taux de réaction sur l'eau est supérieur à 10% donc non négligeable. Entre Vb=0 et la première équivalence, il faut donc tenir compte de deux réactions : celle sur l'eau qui est limitée et celle sur la soude qui est quasi totale (K>>1). Cela dit, puisque le taux de réaction est supérieur à 50% pour Ca=0,01mol/L, ton énoncé veut peut-être de faire dire que la réaction prépondérante est celle sur l'eau dans ce cas et pas dans l'autre cas ; cependant, la réalité est plus complexes car le taux de réaction sur l'eau évolue en fonction de la quantité de soude versée : l'ajout de soude provoque l'apparition de H2A- ce qui déplace l'équilibre de la réaction sur l'eau vers la gauche. Pour Ca=0,01mol/L, le taux de réaction de H3A sur l'eau passe de 55% environ pour Vb=0 à 0% à la première équivalence. Bref : à mon avis tut n'as pas à te préoccuper de cela pour étudier le titrage. Entre Vb=0 et la première équivalence, il suffit de tenir compte des deux réactions (voir document).
Un grand merci pour toutes ces précisions, je comprends bien mieux maintenant !
Par la suite, on nous demande d'écrire les équations de neutralisation de l'acide phosphorique par l'hydroxyde de sodium.
Quand on parle "d'équations" : nous demande-t-on d'appliquer la formule du Ka, les lois de conservation de la matière et de l'électroneutralité pour les réactions suivantes ? Ou bien simplement d'écrire ces réactions ?
H3PO4 + HO− = H2PO4− + H2O
H2PO4− + HO− = H2O + HPO42−
HPO42− + HO− = H2O + PO43−
Merci d'avance !
C'est bien cela ! Attention : seules les deux premières sont quasi totales. On obtient donc deux sauts de pH et pas trois bien qu'il s'agisse d'un triacide... Tout cela est sur le document fourni...
Merci pour cette confirmation !
J'avais bien lu le document en amont, et le fait d'avoir trouvé les mêmes résultats me rassurait un peu (je préférais être sûr de l'avoir bien compris, d'où ma question).
J'aurais une dernière question : on me demande de prédire les valeurs de pH aux demi-équivalences. Si j'ai bien compris le document, il y a 2 sauts de pH, donc 2 équivalences, donc également 2 demi-équivalences ?
J'ai vu que vous aviez traité le problème dans votre document, donc j'appliquerai ensuite votre méthode.
Puisqu'il y a deux équivalences, il y a bien sûr deux demies équivalences, une en Vbe1/2 l'autre en (1/2)(Vbe1+Vbe2) .
L'étude entre Vbe1 et Vbe2 est la seule qui soit simple dans ce titrage. En effet, pour Vb=Vbe1, On obtient une solution de AH2- très peu dissocié dans l'eau. Tout se passe donc entre Vbe1 et Vbe2 comme si on titrait par la soude un monoacide faible initialement peu dissocié. On obtient donc à la deuxième demi-équivalence : pH=pKa2=7,21. (réponse demandée par ton professeur.
En revanche, je me demande si ton professeur a bien conscience de la complexité du problème pour le dosage de la première acidité : l'acide H3A étant initialement fortement dissocié. Pas question donc d'écrire pH=pKa1 à la première demie équivalence. D'ailleurs, pour Ca=0,01mol/L le pH initial est déjà supérieur à pKa1 ! Impossible donc de le prévoir sans calcul. Pour l'obtenir, il faut tenir compte à la fois de la réaction de H3A sur HO- et de la réaction de H3A sur H2O. J'ai fait le calcul paragraphe 3.2 du document...
Merci pour votre réponse, je pense avoir compris !
Concernant la difficulté du problème, j'en discuterai demain avec d'autres étudiants pour savoir comment ils l'ont ressenti. Mon TP ayant lieu demain, on aura peut-être des explications de vive voix de la part du professeur...
En tout cas, vous m'avez vraiment sauvé grâce à vos explications détaillées. Alors une nouvelle fois : un énorme merci pour votre aide et votre temps ! 
Merci ! J'espère que ton professeur n'attend pas comme réponse :
"pH=pKa1 à la première demie équivalence..." 
Je lui poserai la question à la fin du TP : s'il voulait qu'on en déduise cette relation, je vous tiendrai au courant. Quoi qu'il en soit, j'ai bien compris pourquoi ce n'était pas le cas ici.
Bonne soirée à vous 
Rebonsoir,
J'en profite pour faire une mise à jour post-TP : j'ai posé la question, mon professeur attendait bien que l'on dise que pH = pKa1... tout en me disant qu'il savait que c'était une approximation assez grossière. Bref, j'imagine qu'il ne pourra pas me pénaliser pour ça.
Merci encore pour votre aide,
Bonne soirée !


