Inscription / Connexion Nouveau Sujet
Titrage
Bonjour à tous j'ai une question concernant cette exercice pourriez-vous m'aider s'il vous plaît.
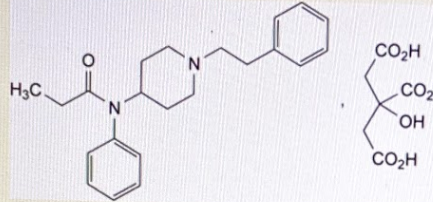
Soit le mode opératoire suivant pour le titrage du citrate de fentanyl. Dissolvez 0,300 g de citrate de fentanyl dans 50 ml d'un mélange de 1 volume d'acide acétique anhydre et de 7 volumes de méthyléthylcétone .
Titrez par l'acide perchlorique 0,1M, Déterminez le point de fin de titrage par potentiométrie.
Pesée et concentration des solutions utilisés
MM du citrate de fentanyl: 528,6
Stoechiométrie : 1 HCIO4 , pour 1 citrate de fentanyl
Pesée de l'chantillon:0,3062 g
Conceniration de la solution HCIO4 01M
Volume lu dans le titrage : 5,34 mL Question Quel est le pourcentage (m/m) du citrate de fentanyl dans l'échantillon titré.
Merci d'avance
Bonjour
On te fournit la stchiométrie de la réaction : à l'équivalence, la quantité d'acide perchlorique ajoutée est égale à la quantité initiale de citrate de fentonyl.
Qu'est-ce qui te gêne dans un cas aussi simple ? Tu n'as même pas à écrire l'équation bilan ni même à remplir un tableau d'avancement...
Citrate de fentyle +1hclo4->
n=m/M c=n/v
0.3/528.6 n= 0.1× 5.34=0.5mol
= 5.67 mol
Je l'ai fait mais la suite je suis bloqué
De la concentration en HClO4 et du volume de cette solution, tu peux déduire la quantité, puis ensuite la masse, de citrate de fentonyle présente dans l'échantillon. Reste alors à comparer cette masse à la masse de l'échantillon : 0,3062 g...
L'énoncé n'est pas des plus clairs effectivement. Je pense qu'il faut comprendre que le volume d'acide ajouté à l'équivalence vaut 5,34mL. Sinon : impossible de résoudre le problème !
Citrate de fentyle +1hclo4->
c=n/v
n= 0.1× 5.34=0.5mol
m=n×M
0.5×528.6=264.3g
Et la comment je compare ma masse?
Tu as laissé le volume exprimé en mL plutôt qu'en litre. Cela fourni une quantité en millimole et donc une masse en milligramme. Il te reste donc à comparer 264,3mg au 306,2mg de l'échantillon...
Je dois calculer le pourcentage (m/m) du citrate de fentanyl dans l'échantillon titré je comprends pas pourquoi il faut comparer les masse


