Inscription / Connexion Nouveau Sujet
Thermodynamique
Bonsoir,
Un récipient placé dans un thermostat a la température T est divisé en 2 compartiment par une paroi amovible. Le1er de volume V1 contient n1 mole de diazote a pression P1 et le second un volume V2 contient n2 mole de dioxygene a pression P2.
1-Evaluer l'enthalpie libre initiale et finale sachant que pour l'enthalpie finale la paroi est enlevé
J'ai besoin d'aide
Je me dit que l'enthalpie libre=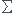 vini
vini
Bonsoir
Si la question se limitait à la détermination de  G, on pourrait utiliser la relation :
G, on pourrait utiliser la relation :
 G=
G= H-T.
H-T. S dans la mesure où la transformation est monotherme.
S dans la mesure où la transformation est monotherme.
Telle que la question est posée, ta méthode me semble être la bonne. je te rappelle que, pour un corps pur, le potentiel chimique se confond avec l'enthalpie libre molaire, pour un corps appartenant à un mélange homogène, le potentiel chimique est l'enthalpie libre molaire partielle.


