Inscription / Connexion Nouveau Sujet
thermo diagramme de clapeyron
bonjour, j'aimerais en savoir un peu plus sur la manière dont fonctionne le diagramme de clapeyron
il me semble qu'il prend en compte la température des corps entre chaque état et à chaque transformation mais l'exercice auquel je suis confronté est un peu particulier car la pression à l'état final est inférieur que celle à l'état initial mais pourtant il se situe plus haut sur le diagramme
voici le sujet de mon exercice:
1 mole d'oxygène se détend d'un volume de 10 L à 25° à un volume de 50 Là 100°.
la détente s'effectue de 2 manière différentes (2 chemins):
chemin a: chauffage isochore suivi d'une détente isotherme
chemin b détente isotherme suivi d'un chauffage isotherme
à quoi dois ressembler le diagramme de clapeyron pour cette situation ?
merci d'avance
Bonjour
En appliquant la loi des gaz parfait, tu vas remarquer que l'état initial (état 1) est représenté dans le diagramme de Clapeyron par un point de coordonnées :
V1=10L ; P1=2,49bar
L'état final (état 2) est représenté par un point de coordonnées :
V2=50L ; P2=0,537bar
Tu peux commencer déjà par placer ces deux points.
Chemin a : pour que la seconde étape soit une détente isotherme à 50°C, il faut commencer par chauffer le gaz de 25°C à 50°C de façon isochore. Cela amène à un point 3 de coordonnées :
V3=V1=10L ; P3=2,69bar
Il te faut ensuite joindre le point 1 au point 3 par une branche d'hyperbole puisque, au cours d'une évolution isotherme, le produit (P.V) reste fixe. L'équation de cette branche d'hyperbole est :
Je te laisse réfléchir à tout cela et continuer...
bonjour, oui hier en refaisant l'exercice (que j'ai réussi), j'ai remarqué mon erreur. le diagramme de clapeyron représente l'évolution de la pression en fonction du volume des différents états du système. mais il dépend brièvement des courbes isothermes de températures. effectivement, p1>p2 mais p1 et p2 sont 2 pressions à 2 températures différentes. il fallait donc que la courbe isotherme à 298 K passe en dessous de celles à 373K. chose que je n'avais pas fait.
j'espère que mon raisonnent est bon ?
j'espère que mon raisonnent est bon ?
Si tu pouvais scanner ton diagramme de Clapeyron, je pourrais vérifier. Il peut effectivement être intéressant ici de tracer les deux branches d'hyperboles correspondant respectivement à 25°C et à 50°C.
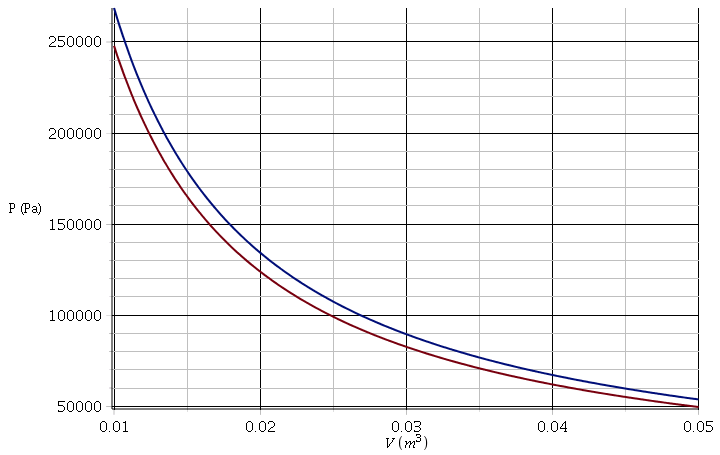
Voici le tracé des deux isothermes ; souvent, pour plus de clarté, on ne respecte pas l'échelle en écartant davantage les deux courbes.