Inscription / Connexion Nouveau Sujet
Thermo
Bonjour j'ai un petit problème avec un exercice . En voila l'ennoncé : "On considère une mole de gaz parfait monoatomique enfermé dans un cylindre fermé par un piston mobile sans frottement de masse négligeable. On supposera que les parois du cylindre laissent passer la chaleur.
Au départ l'ensemble se trouve dans une enceinte où règnent une pression de 1 bar et une température de 277 K. A un instant t, on sort le cylindre de l'enceinte pour le placer dans une pièce où règnent une pression de 1 bar et une température de 298 K (on négligera le temps de transport).
1) Calculer le travail échangé par le gaz au cours de la transformation "
Donc dans la correction , le prof est arrivé jusqu'à : W = 2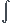 1 -PextdV = - Pext 2
1 -PextdV = - Pext 2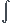 1 dV = -Pext [V2-V1]
1 dV = -Pext [V2-V1]
Jusque là je suis d'accord . Sauf qu'après il a mis :
Pv = nRT, n=1 donc V2 = RT2/P et V1 = RT1/P
donc W = - R [T2 - T1]
Et c'est ce passage là que je ne comprend pas . Comment passons t-on de " -Pext [V2-V1]" à "- R [T2 - T1] "
Si quelqu'un pouvait m'aider , merci d'avance .


