Inscription / Connexion Nouveau Sujet
Squelette sigma
Bonjour
Dans un qcm, on parle de la molecule de cytokine 17 SB 247464 :
Image
(1) L?orbitale atomique contenant le doublet non liant de l?azote 3 est orthogonale ausquelette ?
J?aimerais savoir ce que signifie orthogonale au squelette sigma et dans quel chapitre on voit cette notion
Merci 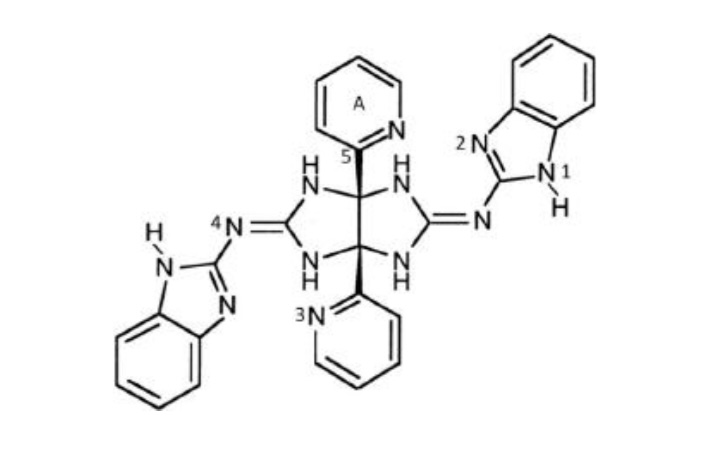
Bonjour
J'ai répondu à une question analogue à propos de l'hybridation de N. Tu as ici une hybridation sp2 ; les trois orbitales sp2 ont leurs axes orientés dans un même plan à 120° les unes des autres. Ces orbitales sont occupées de la façon suivantes :
* 2 de ces orbitales possèdent chacune un électron permettant l'établissement de 2 liaisons  avec les deux atomes C voisins, ce qui conduit à un cycle plan avec angles de liaisons de 120° (comme pour le benzène). Ce cycle formés d'atomes liés par liaisons
avec les deux atomes C voisins, ce qui conduit à un cycle plan avec angles de liaisons de 120° (comme pour le benzène). Ce cycle formés d'atomes liés par liaisons  peut être appelé squelette
peut être appelé squelette  .
.
* la troisième orbtale sp2 est occupé par le doublet de valence non liant.
Reste donc l'orbitale pz occupé par un électron. Chacun des 5 atomes C et de l'atome N possède ainsi chacun un électron  occupant ainsi chacun une orbitale
occupant ainsi chacun une orbitale  . Il va donc y avoir délocalisation des 3 liaisons
. Il va donc y avoir délocalisation des 3 liaisons  . La structure est aromatique.
. La structure est aromatique.
Contrairement à ce que tu as écrit : l'orbitale pz est occupée par un seul électron. S'il n'en était pas ainsi, le cycle contiendrait 7 électrons  , la structure ne serait pas aromatique.
, la structure ne serait pas aromatique.
Ce cycle est équivalent à celui de la pyridine illustré ici : ![]()
L'orbitale pz est représenté en mauve et jaune. La troisième orbitale sp3 contenant le doublet libre est représentée en vert.


