Inscription / Connexion Nouveau Sujet
Spectre de Balmer de l'atome d'hydrogène
Bonjour, j'ai besoin d'aide :
La formule ci contre, dite de Rydberg-Ritz, donne les longueurs d'onde des raies caractéristiques de l'atome H, où  est la longueur d'onde dans le vide, RHla constante de Rydberg de l'atome H, n1 et n2 entiers (n1
est la longueur d'onde dans le vide, RHla constante de Rydberg de l'atome H, n1 et n2 entiers (n1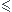 n2)
n2)
1/ = RH(
= RH( -
)
On donne pour la série de Balmer (n1=2) :
H : 656 nm
: 656 nm
H : 486 nm
: 486 nm
H : 434 nm
: 434 nm
H : 410 nm
: 410 nm
H : 397 nm
: 397 nm
1)Vérifier cette loi par tracé d'une droite, et en déduire la valeur de RH dans le SI
La série de Balmer correspond à des transitions entre le niveau n2 et n1=2.
La raie H correspond à n2=3, H
correspond à n2=3, H à n2=4, etc. Plus les niveaux d'énergie sont éloignés, plus la longueur d'onde est faible (E=hc/
à n2=4, etc. Plus les niveaux d'énergie sont éloignés, plus la longueur d'onde est faible (E=hc/ ).
).
Il faut donc tracer 1/ en fonction de 1/n22, et vérifier qu'il s'agit bien d'une droite.
en fonction de 1/n22, et vérifier qu'il s'agit bien d'une droite.


