Inscription / Connexion Nouveau Sujet
Solution
Bonjour,
J'ai un exercice de chimie pour la rentré mais je n'y pige rien.
Donc si quelqu'un pourrais m'aides sa serais super.
Voici l'exercice:
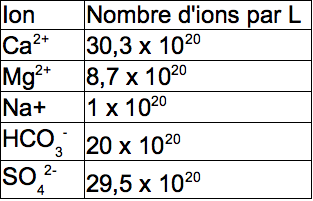
Montre que cette solution est électriquement neutre. Attention, réfléchis !
Bonjour.
pour commencer, il faut detecter le nombre de charges de chaque type d'ion.
Ensuite calcules le nombre total de charge positive( pour les cations) et celui des charges negatives(anions). En principe, tu dois trouver le même nombre en valeur absolue.
exemple: pour Na+ on a: (2*30.10 exposant 20) charges positives.
essai la suite....
Déjà, merci de ta réponse.
Mais vois tu, j'ai un professeur de physique qui nous apprends rien. Il nous donne des exercices sans nous expliquer. C'est pourquoi dans ta réponse il y a des mots que je ne connaissais pas comme "cations" et "anions".
Et calculer je ne sais même pas d'ou sortent certains chiffre !!!
salut;
avant tout propos, garde un respect pour ton prof car tes qualifications ( je cite:" j'ai un professeur de physique qui nous apprends rien.") ne sont pas bonnes.
Anion veut dire ion negatif et les cations sont des ions positifs.
Dis moi; comprends-tu au moins ce qu'on appelle la charge d'un ion?
Bonjour!
Pas trop ça, disons que cette charge dépend effectivement du nombre d'électrons perdus ou gagnés.
Passons maintenant a la résolution de ton exercice:
Calculons la charge totale des charges positives(pour les 3 premiers ions dans le tableau):
2x30,3.10^20 +2x8,7. 10^20 +1. 10^20 = 79. 10^20
Pour les charges négatives(les deux derniers ions dans le tableau) : 20.10^20 + 2x29,5.10^20 = 79.10^20
Conclusion : visiblement le nombre de charges positives est égale au nombre de charges négatives : la solution est alors électriquement neutre
j'espère que cela pourra t'aider....


