Inscription / Connexion Nouveau Sujet
Reactif, pression, tableau d'avancement...
Coucou !
P'tit probleme de chimie...Si on pouvait m'aider !
Enoncé:
Dans un flacon de 200mL, on fait réagir 40mL d'acide chlorydrique, de concentration 1,00mol.L-1avec un morceau de calcaire de masse m=8.50g
L'equation de la reaction s'écrit: 2H++CaCO3 Ca2++CO2+H2O
Ca2++CO2+H2O
On estime la temperature a l'etat initial et a l'etat final est la meme et est egale a 25°C
1)a/ Quelle est la pression de depart dans le flacon?
b/ Comment va evoluer la pression dans le flacon tout au long de la reaction?Pourquoi?
2)a/Determiner les quantités de matiere initiale des reactifs
b/ Elaboré le tableau d'avancement
c/ Quel est le reactif limitant?
3)a/Determiner la supression de  P dans le flacon
P dans le flacon
b/En deduire la pression dans le flacon
Mon raisonnement:
1)a/ Quelle est la pression de depart dans le flacon?
PV=nRT Donc P= nRT/V
P=(0.04*0.31*(273+25))/0.04
P 2,47.103
2,47.103
La pression de depart est environ egale a 2,47.103
b/ Comment va evoluer la pression dans le flacon tout au long de la reaction?Pourquoi?
Si la temperature est consta,nte tout au long de la reaction, la pression sera elle aussi constante...
2)a/Determiner les quantités de matiere initiale des reactifs
nacide= cV
= 1*40.10-3
=0.04 mol
ncalcaire=m/M
= 8.50/ (40+12+3*16)
=0.085 mol
b/ Elaboré le tableau d'avancement
c/ Quel est le reactif limitant?
Les rapports des quantités initiales aux nombres stoechiometrique correspondant sont:
nacide/1=0.085 et ncalcaire/2=0.02
Comme ncalcaire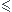 nacidealors le reactif limitant est l'acide (2H+)
nacidealors le reactif limitant est l'acide (2H+)
3)a/Determiner la supression de  P dans le flacon
P dans le flacon
C'est quoi  P ??
P ??
[b]b/En deduire la pression dans le flacon
Je ne sais pas comment faire...
)a/ Quelle est la pression de depart dans le flacon?
PV=nRT Donc P= nRT/V
P=(0.04*0.31*(273+25))/0.04
P2,47.103
bonsoir!
unité?
b/ Comment va evoluer la pression dans le flacon tout au long de la reaction?Pourquoi?
Si la temperature est consta,nte tout au long de la reaction, la pression sera elle aussi constante...
justifie, parle de la loi de Boyle-Mariotte
2)a/Determiner les quantités de matiere initiale des reactifs
nacide= cV
= 1*40.10-3
=0.04 mol
ncalcaire=m/M
= 8.50/ (40+12+3*16)
=0.085 mol
b/ Elaboré le tableau d'avancement
c/ Quel est le reactif limitant?
Les rapports des quantités initiales aux nombres stoechiometrique correspondant sont:
nacide/1=0.085 et ncalcaire/2=0.02
Comme ncalcairenacidealors le reactif limitant est l'acide (2H+)
Merci pour tout sa !!
Ce qui me pose probleme, c'est surtout ses 2 questions:
3)a/Determiner la supression de
 P dans le flacon
P dans le flacon
b/En deduire la pression dans le flacon
Car je ne c'est pas se qu'est  P donc je ne vois pas comment le supprimer et pareil, plus haut j'ai dit que la pression etait constante, donc comment deduire la pression du fklacon?
P donc je ne vois pas comment le supprimer et pareil, plus haut j'ai dit que la pression etait constante, donc comment deduire la pression du fklacon?
Determiner la supression de P dans le flacon
Déjà comprends-tu la question à part delta P?
Nan, c'est justement cela le souci...
Cela veux dire, qu'a la fin il n'y a plus de pression?
Car a la base, la pression est constante et vaut P=2,47.103 Pa...
Etc'est la que je ne comprend plus, elle est constante et ensuite on nous dit qu'elle est supprimé !! 
Je suis perdue...
Ba comme dans la question 3), on nous parle de surpression, c'est que la pression augumente mais dans l'enoncé,la temperature reste constante oui...
Coucou !
P'tit probleme de chimie...Si on pouvait m'aider !
Enoncé:
Dans un flacon de 200mL, on fait réagir 40mL d'acide chlorydrique, de concentration 1,00mol.L-1avec un morceau de calcaire de masse m=8.50g
L'equation de la reaction s'écrit: 2H++CaCO3Ca2++CO2+H2O
On estime la temperature a l'etat initial et a l'etat final est la meme et est egale a 25°C
1)a/ Quelle est la pression de depart dans le flacon?
b/ Comment va evoluer la pression dans le flacon tout au long de la reaction?Pourquoi?
3)a/Determiner la supression de P dans le flacon
b/En deduire la pression dans le flacon
Mon raisonnement:
1)a/ Quelle est la pression de depart dans le flacon?
PV=nRT Donc P= nRT/V
P=(0.04*0.31*(273+25))/0.04
P=2,47.103 Pa
La pression de depart est environ egale a 2,47.103 Pa
b/ Comment va evoluer la pression dans le flacon tout au long de la reaction?Pourquoi?
Si la temperature est consta,nte tout au long de la reaction, la pression sera elle aussi constante...
3)a/Determiner la supression de  P dans le flacon
P dans le flacon
Je ne comprend pas du tout cette question...peut on m'aider
b/En deduire la pression dans le flacon
Au debut c'est constant, donc je ne comprend plus rien...
*** message déplacé ***
Peux tu me donner la formule du calcaire qui t'es donné dans l'énoncé ? Je ne trouve pas la même chose que toi...
*** message déplacé ***

 suppression
suppression




