Inscription / Connexion Nouveau Sujet
Questions sur la règle de l'octet
Bonsoir,
Je me pose quelques question quant à la règle de l'octet.
Tout d'abord, elle n'est applicable que sur les atomes dans une molécule électriquement neutre ?
Ensuite pour la molécule (électriquement neutre), l'une des représentations de Lewis est :
/ \
|O - N = O ici O (de gauche) et N ne respectent pas la règle de l'octet (d'où (+) et (-) ) ...
\ . /
(-) (+)
l'autre étant :
/ _ \
O - N = O ici "tout le monde" respecte la règle.
\ /
.
Une dernière chose, la raison pour laquelle on n'a pas : = N = est qu'un élément de la seconde période ne peut former que 4 liaisons maximum. Pourquoi ça ?
.
(source pour les représentations : http://departements.univ-reunion.fr/chimie/briere/sujcor/Juin03/juin03NO2cor.htm)
J'ai sûrement dit des choses fausses et j'aimerais bien savoir lesquelles.
Merci d'avance.
Bonjour,
seuls les éléments du bloc p de période n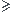 3 peuvent être entourés de plus de 8 éléctrons.
3 peuvent être entourés de plus de 8 éléctrons.
N étant un élément de la 2ème période est ne peux pas avoir plus de 8 éléctrons (et donc pas plus de 4 liaisons)
Bonne soirée 


