Inscription / Connexion Nouveau Sujet
Propriétés des amines
bonjours, pouvez vous m'aider à repondre quelque question svp?
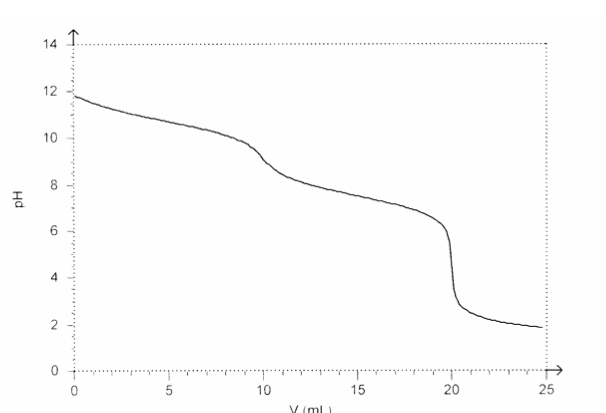
On dose V0 = 10 mL d'une solution d'éthylènediamine de concentration C0 par une solution d'acide chlorhydrique de concentration CA = 0,10 mol.L-1. On note V le volume d'acide chlorhydrique versé. On suit la réaction de dosage par pHmétrie et on obtient la courbe de dosage tracée page suivante
a- Décrire le montage expérimental permettant de réaliser un tel dosage. On précisera en particulier la nature et le rôle de chaque électrode.
b- Justifier l'existence de deux sauts de pH. Lequel convient-il d'exploiter ?
c- Écrire les équations des réactions de dosage caractérisant chaque partie de la courbe.
d- Déterminer la concentration C0 en éthylènediamine de la solution à doser.
T'es en Terminale S ? C'est un sujet de maths sup maths spé ^^. Je m'y suis mis y a 5 mins et j'avoue qu'il est pas si facile. Pour l'existence des 2 sauts je pense que c'est dû aux deux couple redox présents. HCL/Cl- et C2H4(NH2)2/C2H9N2+
J'avance un peu dans mes recherches :p En pH métrie, la plupart du temps on utilise 2 électrodes, une de référence qui garde un pH constant et donne le pH de la solution acqueuse et une électrode de mesure qui va varier suivant le pH.
Il n'y a pas de couple redox la dedans .Il n'y a que des réactins acidobasiques
la formule de l'éthylènediamine est 2HN-CH2-CH2-NH2 qui est une dibase . Quand on ajoute progressivement des iions H+ ( acide fort) on a succesiivement les 2 réactions : (1) 2HN -CH2-CH2-NH2 + H+ -> +H3N-CH2-CH2-NH2 puis (2) +3HN-CH2-CH2NH2 + H+ -> =3HN-CH2-CH2-NH3+
le premier saut correspond à la fin de la première réaction et le deuxième saut correspond à la fin de la deuxième réaction.
il est evident que ce deuxième saut est plus explitable et qaund on arrive à cette équivalence on a mis 2H+ pour 1 ethylènediamine au départ




