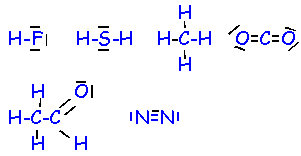Inscription / Connexion Nouveau Sujet
probleme de chimie......
Bonjour!! j n'&rrive pas a faire la representation de Lewis du fluorure d'oxygene. Est-ce que quelqu'un peut me donner des indications svp?? merci.
Bonjour et bonne année!
A moins que ton prof soit en avance tu aurais du poster dans la rubrique "lycée".
Le fluorure d'hydrogène est constitué d'atome de fluor et d'hydrogène.
Cherche sa formule tout d'abord, ensuite tu recherches le nb d'électrons périphériques (sur la couche externe).
Tu dessines les doublets liants et non-liants et tu fais ta représentation.
patiente deux secondes j'ai un doute sur la formule je préfère vérifier. Je dirais HF mais bon...
En effet je confirme, tu n'as pas la représentaion de Lewis mais tu as sa formule développée...
Pour le fluor, Z=9. Donc la formule électronique de l'atome de fluor est: (K)2(L)7. L'atome de fluor possède 7 électrons dans sa couche externe. Alors l'atome de brome, appartenant à la même famille possède aussi 7 électrons dans sa couche externe.
(On n'est pas obligé de passer par la formule électronique du fluor pour répondre à la question. Il est aussi rapide,sinon plus rapide, de dire que, si le fluor est dans la colonne 7 de la classification périodique simplifiée, l'atome de fluor possède 7 électrons dans sa couche externe).
A toi
ben oui ca j'avais trouvé mais ( euh oui je me suis trompé d'endroit  ) c'est pas logique que le fluor doive acquerir 7 electrons!! enfin, moi ca me parait fou. j'essaye la representation, mais je ne vois pas comment!
) c'est pas logique que le fluor doive acquerir 7 electrons!! enfin, moi ca me parait fou. j'essaye la representation, mais je ne vois pas comment!
Bonsoir!
Personne n'a pas écris que le fluor devait acquérir 7 électrons mais qu'il en possède 7 sur sa couche externe. Pour rappel: ce sont ces électrons que l'on représente dans la repésentation de Lewis.
As-tu encore des questions?
oui, en ait j'ai trouvé, je me suis trompé dans la structure electronique!! merci quand meme!!!
bonne soirée, cordialement, Aragas
merci theidiot, je me suis absentée désolé, vraiment merci d'avoir pris le relais...
entre parenthèses à ma connaissance aucun atome n'est suffisamment électronégatif pour attirer 7 électrons!
Tu as fini par trouver Aragas?
7 électrons donc 3 doublets non-liants et un liant.
Tu as donc 3 traits et un point autour du fluor
oui j'ai trouvé merci en fait je m'étais trompé dans la structure élécrtonique. merci pour la representation mais c'est pas la bonne!! c'est OF2, et non HF !!!
On l'appelle également acide fluorhydrique si ma mémoire est bonne 
Ce que tu as nommé est du difluorure d'oxygène...
Ds ton autre topic tu avais mis fluorure d'hydrogène masi bon. Evite de monter sur des gds chevaux stp sinon tu te débrouilles tt(e) seul(e)...
L'oxygène possède combien d'électrons sur sa couche externe?
désolée de m'être emporté!!
j'ai fini mon DM aujourd'hui, je pense avoir trouvé même avec une fausse formule!!
merci quand même!!
Pour F2O
O a deux doublets liants et deux doublets non liants. F a trois doublets non-liants et un liant.
- - -
|F - O - F|
- - -
Voila j'espère que tu comprends
désolé à moi...
Ok et bien bonne soirée, bonne continuation j'espère...
J'espère que tu ne garderas ni un mauvais souvenir du forum, ni un mauvais souvenir de moi parce-que nous avons eu un petit accrochage...
Adishatz