Inscription / Connexion Nouveau Sujet
potentiel hydrogène
Bonjour,
J'ai vraiment du mal avec un exercice.
On veut réduire pour réduire la concentration des Ca2+ dans une eau dure de 10-3 moles/L à 10-10 moles/l . A quel pH faut-il ajouter une solution d'EDTA pour obtenir cette réduction de concentration.
A) pH = 5
B) pH = 12
C) pH = 13
D) pH = 3
E) pH = 1
Mon raisonnement : J'ai pas vraiment compris l'exercice. Je sais juste que pH = - log [H30+]
ou même [H3O+] = 10^-pH
EDTA = sel disodique dihydraté est un chélateur de cations divalents.
je vois pas trop comment faire j'ai besoin qu'on me donne des indices ou qu'on m'éclaire un peu
cordialement
ZOHRA
Bonjour
L'EDTA peut complexer les ions calcium de façon quasi totale pour :
pH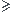 10.
10.
Il faut aussi faire attention à ce qu'un pH trop basique n'entraîne pas une précipitation sous forme d'hydroxyde de calcium...
Bref : pour trancher entre les réponses B et C il faut des renseignements complémentaires : le produit de solubilité de l'hydroxyde de calcium par exemple.


