Inscription / Connexion Nouveau Sujet
Nitrobenzène et addition d'eau
Bonjour,
j'aurais une question par rapport aux effets électroniques du phényle.
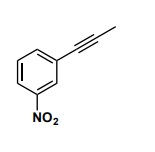
Cette molécule ci-dessous régit avec de l'eau en milieu acide. Donc addition d'eau.
Cette réaction suit la règle de Markovnikov. Ici le "nitrophényle" possède un effet -I et -M. Donc l'hydrogène ira en priorité sur le carbone "de gauche" du groupement alcyne, pour former le C+ le plus stable.
Maintenant imaginons que le groupement NO2 ne soit plus là. On aurait le groupement phényle seul lié à l'alcyne. L'effet inductif du phényle est -I. Mais son effet mésomère est-il -M ou +M ?
Je dirais +M, et dans ce cas là l'H irait sur le carbone "de droite", pour former le C+ le plus stable.
Merci d'avance.
Bonjour Pierre33 :
Hydratation d'un alcyne :
Lors de la fixation d'eau sur un alcyne , on obtient un énol ( catalysé avec H3O+/HgSO4 ) .
( La fixation de H-OH obéit à la règle de Markovnikov ) . L'énol instable s'isomérise en cétone
plus stable . On obtient finalement une cétone et c'est seulement avec l'éthyne que l'on obtient
un aldéhyde : soit l'èthanal .
Je pense que dans ton cas on obtient du 3`-nitroacétophénone .
Sans le groupe nitro , cela devrait -être la même chose .
Bonnes salutations .
bonjour pierre33 :
Je m'excuse , mais j'ai fait erreur en indiquant le produit 3`-nitroacétophénone !
Il s'agit du 3-nitrophénylacétone .
Sans le groupe nitro on obtient la phénylacétone .
Bonnes salutations .
Bonjour,
je te remercie pour ta réponse.
Avec le groupe nitro a priori on trouve la même chose.
Par contre sans le groupe nitro je ne vois toujours pas pourquoi ça devrait être identique.
Le groupement phényle n'aurait-il pas un effet +M sur le carbocation si l'H attaquait le carbone de droite ? Donc il serait le plus stable et on obtiendrait du phénylpropanone (?).
En espérant que tu puisses m'éclaircir les idées.
Merci encore.
Bonsoir pierre33 :
Phénylacétone ou phényl-2-propanone ( = même chose ) .
Je ne sais pas si sans le groupe nitro ( électrophile , attracteur d'électrons ) , dans
le groupe phényl , peut jouer un rôle inductif ?
C'est un cas difficile ( on peut aussi imaginer une isomérisation allènique de la
triple liaison C≣C−C ou C=C=C ) .
Si tu trouves une bonne explication , je serai intéressé de la connaître .
Autre chose :
Comment peux-tu dessiner proprement les structures chimiques ?
Moi je ne peux pas le faire avec mon Mac .
Bonnes salutations .
C'est un cas difficile ( on peut aussi imaginer une isomérisation allènique de la triple liaison C≣C−C ou C=C=C )
Je n'ai pas d'énormes connaissances en chimie ; là je ne comprends pas

C'est un exercice d'annale, je ne pense pas que la prof avait en tête quelque chose d'aussi compliqué.
Comment peux-tu dessiner proprement les structures chimiques ?
Je ne sais pas, j'ai juste copié la molécule présente dans le sujet ...
Je vais demander à ma prof, pas sur qu'elle me réponde par contre.
Rebonsoir pierre33 :
J'ai cherché et j'ai trouvé le produit allènique que voici .
Benzene, 1-nitro-3-(1,2-propadienyl)- | C9H7NO2 - PubChem - NIH
https://pubchem.ncbi.nlm.nih.gov/compound/13257084 - Traduire cette page
Benzene, 1-nitro-3-(1,2-propadienyl)- | C9H7NO2 | CID 13257084 - structure, chemical names, physical and chemical properties, classification, patents, literature, biological activities, safety/hazards/toxicity information, supplier lists, and more.
méta-( -1-nitro - C6H4-)- position- 3-CH=C=CH2 .
Malheureusement je ne peux pas le dessiné ( C6H4 - est le benzène disubstitué ) .
Essaye de trouver la référence .
Bonnes salutations .
Bonjour,
d'accord je te remercie.
Donc si je comprends bien, le H+ peut attaquer un des 2 carbones indépendants, il sera stabilité par effet l'effet +M de la 2e liaison double.
J'ai envoyé mon mail à ma prof, je te tiens au courant de ce qu'elle dira.
Hop double post.
J'ai eu sa réponse : le phényle (qu'il y est le nitro ou pas ça ne change rien), aura un effet +M.
Donc on obtiendra majoritairement le 1-nitrophénylpropan-1-one.
Bonsoir pierre33 :
Merci pour ta réponse ; en effet dans ce cas lors de l'addition d'une molécule d'eau sur la
triple liaison , le groupe -OH va s'additionner en conjugaison avec le cycle aromatique puis
la forme énolique s'isomérise en cétone pour donner le 3-nitrophénylpropan-1-one et pas
le 3-nitrophénylpropan-2-one .
En effet l'absence du groupe nitro ne change en rien .
C'était un problème de chimie intéressant . Bonnes salutations .


