Inscription / Connexion Nouveau Sujet
Molécule de nicotine
Bonjour
J'ai une question par rapport a la molécule de nicotine et son enantiomere;
Enantiomere = image mirroir non superposable
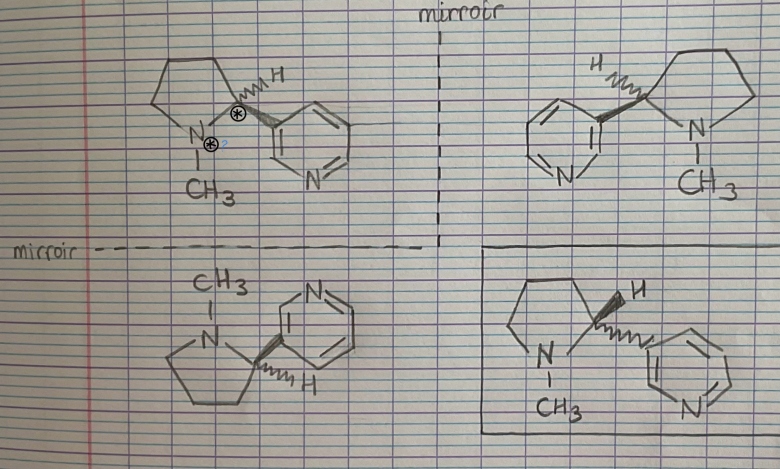
Mais on peut faire plusieurs image mirroir d'une molecule (ca depend d'ou on place le mirroir) img
Dans cette image toutes les images mirroirs sont des enantiomeres ou il y a seulement 2 enantiomere
Egalement le N avec l'asterix est-il un N asymetrique car j'avais l'impression qu'il avait 3 grp differents et un doublet non liant
Merci
Bonsoir
C'est vrai que, suivant la position du miroir, la représentation de l'image n'est pas la même mais la question n'est pas là : cette molécule image : est-il possible, par rotation, retournement, etc... de la superposer à la molécule objet ? La réponse, pour une molécule objet donnée, est unique, quelle que soit la position du miroir.
Ou alors le nb d'enantiomere depend du nb centre chiral
Pour un centre chiral la situation est simple : la molécule est chirale donc cela donne un couple d'énantiomère.
Pour plusieurs centre chiraux, la situation est plus complexe : malgré l'existence de ces centres chiraux, des symétries peuvent rendre la molécule non chirale.
Une chose simple tout de même : soit la molécule est chirale, soit elle ne l'est pas. Si elle est chirale, on obtient un couple d'énantiomères, quel que soit le nombre de centres chiraux. Si elle ne l'est pas, pas d'énantiomères.
Merci pour votre reponse vanoise,
Ou alors le nb d'enantiomere depend du nb centre chiral
Pour un centre chiral la situation est simple : la molécule est chirale donc cela donne un couple d'énantiomère.
Pour plusieurs centre chiraux, la situation est plus complexe : malgré l'existence de ces centres chiraux, des symétries peuvent rendre la molécule non chirale.
Une chose simple tout de même : soit la molécule est chirale, soit elle ne l'est pas. Si elle est chirale, on obtient un couple d'énantiomères, quel que soit le nombre de centres chiraux. Si elle ne l'est pas, pas d'énantiomères.
Je viens de voir que pour trouver le nb d'enantiomers il faut appliquer la formule : 2n (n = nb de centre chiraux)
Sachant que chaque carbone asymétrique peut être R ou S, cela donne effectivement 2n possibilités de carbones asymétriques mais cela ne signifie pas nécessairement autant de molécules chirales et deux fois moins de couples d'enantiomeres.
Des symétries dans les molécules peuvent réduire ces nombres. Par exemple, la molécule d'acide tartrique possède deux C* . Cela conduit à un seul couple d'énantiomeres et à une molécule non chirale.
Bonjour
Juste pour être sur j'aimerais recapitulé ce que j'ai compris (cela m'aide a retenir et j'aimerais être sur d'avoir bien compris)
Donc une molecule peut avoir plusieurs images mirroirs (dependant d'ou on place le mirroir) il faut faire des rotation verticales, horizontale et les faires tourner a ces images mirroirs pour voir si on retrouve la molecule de depart - (on peut se contenter de dessiner une seule image mirroir) - le nombre d'enatiomeres depend de la molecule (certaines peuvent en avoir plusieurs d'autre non)
Des symetrie dans la molécule peuvent reduire le nb d'enatiomeres (les molecules symetrique ne sont pas optiquement actives alors que les enantiomeres si donc une molecule ayant une symetrie ne peut être un enantiomere)
Mais s'il n'y a pas de symetrie le nb d'enantiomeres vaut 2n avec n le nb de centre chiraux
Merci beaucoup pour vos reponses, elles m'aident enormement a comprendre