Inscription / Connexion Nouveau Sujet
metaux usuels
bonsoir
le fer brule dans le dioxygene pour donner l'oxyde magnetique
1. ecrire l'équation bilan de la reaction
2. on met en presence 11.2g de fer et 4.8g de dioxygene.
a) determiner le reactif en excés
b) calculer la masse d'oxyde de fer a la fin de la reaction
c) calculer la masse restante du reactif utilisé en excés
ma solution
1.
3Fe + 2O2  Fe3O4
Fe3O4
2.
a)
n(fer)=m/M=11.2/56=0.2mol
n(O2)=m/M=4.8/32=0.15mol
or 3mol de fer reagissent avec 2mol de dioxygene
donc comparons n(fer)/3 et n(O2)/2
n(fer)/3=0.2/3=0.07mol et n(O2)/2=0.15/2=0.075mol
on a donc 0.07mol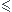 0.075mol d'ou le dioxygene est en excés
0.075mol d'ou le dioxygene est en excés
b)
n(Fe3O4)=0.07mol donc m=n*M=0.07*232=16.24gramme
c)
le nombre de mol de O2 necessaire =2*n(Fer)/3=0.07*2=0.14mol
la masse correspondante=0.14*32=4.48gramme
la masse restante du reactif en excés=4.8-4.48=0.32gramme
pour le c) quand je calcule le nombre de mol qui n'a pas reagit=0.075-0.07=0.005mol
et la masse qui n'a pas reagit=0.005*32=0.16gramme
je me demande pourquoi je ne trouve pas le meme resultat concernant la masse restante.
aidez moi s'il ya des erreurs
bonjour
sil vous plait pouvez vous m'expliquer pourquoi dans la question c) la premiere methode n'est pas bonne.
je ne comprends pas réellement

 !
!

