Inscription / Connexion Nouveau Sujet
Les peintures dépolluantes
bonjour, je passe en MP et pour les vacances les profs nous ont donné quelques exos à travailler. J'ai terminé la plupart mais il m'en reste 2 où je suis bloqué, un en chimie et un en physique.
Voici celui de chimie:
TiO2 se comporte comme un photocatalyseur. Il existe essentiellemnt sous deux formes allotropiques: rutile et anatase.
J'ai fait la partie A .
Partie B: étude de l'équilibre d'adsorption du polluant: une expérience est menée en solution aqueuse, il s'agit de l'adsorption sur TiO2 de l'hélianthine notée H, de masse molaire 305g/mol. L'équilibre considéré est MM+H(aq)=M-H-M avec MM le site d'adsorption entre deux atomes et M-H-M le molécule chimisorbée. A 298K , K3=18940 et à 308K, K3=25080.
1)Exprimer la constante d'équilibre K3 en fonction des activités des espèces mentionnés.
est ce qu'il suffit juste de mettre K3=a(M-H-M)/a(MM)*a(H) ??
2)Déterminer l'enthalpie standard de la réaction supposée indépendate de la température.
Je ne sais pas comment faire
Partie C:cinétique de dégradation du polluant: toujours avec l'hélianthineon effectue une série de mesures de concentration en fonction du temps (à 298K).L'hélianthine est initialement à la concentration de 12.0mg/L
temps d'irradiation(h)->concentration (mg/L)
1->8.89
2->6.59
3->4.64
4->3.44
6->1.79
8->0.985
1)Montrer que la réaction est d'ordre 1 par rapport à l'hélianthine.
J'ai fait le graphe des résultats obtenus concentration en fonction du temps. On a v=k[H]p[MM]q. Je pensais faire l'hypothese d'ordre 1 pour l'hélianthineet vérifier que ce que je trouve corrsepond aux résultats expérimentaux mais je sais pas quoi faire du [MM]q. est ce que je peux faire hypothèse d'ordre 0 pour MM??
2)déterminer la constante de vitesse de la réaction
Je pense que je peux me débrouiller avec cette question si je trouve celle d'avant
Merci pour votre aide et bonne journéé
jo
Bonjour,
1)Exprimer la constante d'équilibre K3 en fonction des activités des espèces mentionnés.
est ce qu'il suffit juste de mettre K3=a(M-H-M)/a(MM)*a(H)?
Je dirais non car il faut connaître les états de MM et M-H-M.
a(MM)s = 1 donc il faut regarder le sujet.
SI seul H est indiqué aqueux , je pense que
2)Déterminer l'enthalpie standard de la réaction supposée indépendate de la température.
Je ne sais pas comment faire
J'aurais utilisé la loi de Van't Hoff
1)Montrer que la réaction est d'ordre 1 par rapport à l'hélianthine.
Tracer le graphique Ln (C) = f(t) si les points sont alignés et que le coefficient r² de la une régression linéaire
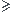 0,999 alors c'est une réaction d'ordre 1 par rapport à H.
0,999 alors c'est une réaction d'ordre 1 par rapport à H.
Je l'ai fait sur excel c'est nickel.
v=k[H]p[MM]q
 constant ; l'ordre est dégénéré (je crois que c'est le terme).
constant ; l'ordre est dégénéré (je crois que c'est le terme).
2)déterminer la constante de vitesse de la réaction
Avec le graphique, la pente sera -k.
Bonjour,
Je suis exactement dans la même situation que jodusud.
J'ai réussi de même les premières questions et suis bloqué à celle de l'enthalpie.
Citation :
2)Déterminer l'enthalpie standard de la réaction supposée indépendate de la température.
Je ne sais pas comment faire
J'aurais utilisé la loi de Van't Hoff
Je ne comprends pas bien comment vous pouvez passer de cette loi pour obtenir l'enthalpie standard au final.
Pourriez-vous m'éclaircir quelque peu sur ce point svp ?
Merci d'avance !
Bonne soirée
Bonjour,
Je ne comprends pas bien comment vous pouvez passer de cette loi pour obtenir l'enthalpie standard au final.
J'ai bien écrit J'aurais utilisé.
De mémoire, Ea est l'énergie d'activation. Est-ce le même terme qu'enthalpie standard ? C'est bien pour ça que j'ai écrit au conditionnel.
Sinon mon raisonnement :
En espérant que cela vous aide.
Ea j ai aussi appris ca comme etant l energie d activation. je ne sais pas du tout si c'est pareil que l'enthalpie standard. Si c'est bien cela, alors ce n'était pas compliqué
Bonjour,
J'ai regardé quelques autres pages sur internet, et apparemment il semblerait que vous ayez bien raison.
L'énergie d'activation serait l'augmentation d'énergie nécessaire à la formation de la réaction d'après ce que j'ai pu comprendre.
http://mendeleiev.cyberscol.qc.ca/chimisterie/chimie534/graph.htm (Premier graphique)
Donc il fallait le savoir ^^
Merci en tout cas pour cette aide, et pardonnez mon scepticisme 
Bonne journée


