Inscription / Connexion Nouveau Sujet
Le tungstène (vérification)
Bonjour, ce serait pour une vérification et éventuellement un complément :
1. On donne les abondances isotopiques relatives de l'élement tungstène :
180W : 0,13%
182W : 26,3%
183W : 14,3%
184W : 30,67%
186W : 28,6%
Déterminer, à une décimale près, la masse molaire du tungstène.
2. Son numéro atomique est Z=74. Donner la configuration électronique attendue de l'atome à l'état fondamental.
______________________________________________________________
1. J'utilise la formule
M = 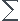 xi*Ai où xi est la % de chaque isotope et Ai sa masse molaire associée.
xi*Ai où xi est la % de chaque isotope et Ai sa masse molaire associée.
M = 0,0013*180 + 0,263*182 + 0,143*183 + 0,3067*184 + 0,286*186
M = 183,9 g/mol.
2. La configuration à l'état fondamental
n'a-t-elle pas une exception ?
_____________
Merci pour vos réponses 
bonsoir,
1- OK
2- comme configuration électronique attendue à l'état fondamental je donnerai
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d4
mais je ne sais pas s'il y a une exception dans le cas du tungstène.
En règle générale la couche d est plus stable quand elle est moitié remplie et là elle ne possède que 4 électrons (au lieu de 5 pour être à moitié pleine)
dans wikipédia, ils n'ont pas mis les couches dans l'ordre de remplissage (c'est pas toujours une source très fiable) mais niveau structure ils ont donc la même que celle que je proposai.
Ceci dit à de tels nivaux, l'ordre de remplissage n'est pas toujours respecté


