Inscription / Connexion Nouveau Sujet
Le cycle de Hess
Bonjour,
J'ai un gros problème de compréhension sur le cycle de Hess, dans plusieurs exercices je ne comprend pas les signes utilisés. Alors je vous présente mon exo:
Calculer l'enthalpie de formation standard de l'eau liquide.
On donne à 25°C: Energie de liaison de H2 = 436 kJ/mol; O2= 468 kJ/mol
Enthalpie de vaporisation de H2O(l) = 40 kJ/mol
Energie de liaison O-H = 455 kJ/mol
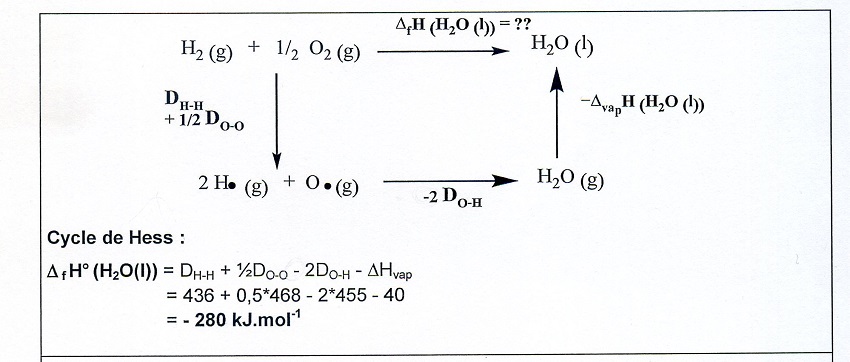
La solution de l'exercice étant l'image que j'ai inséré.
Ce que je ne comprend pas c'est le moins que l'on met à -2 DO-H, en fait je ne comprend pas aussi pourquoi on met cette énergie de liaison.
Merci d'avance