Inscription / Connexion Nouveau Sujet
Evaporateur
Bonsoir,
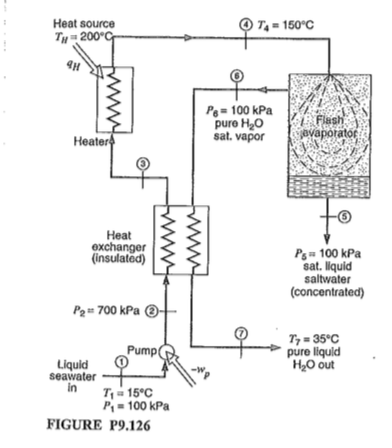
On s'intéresse ici à un process qui fournit de l'eau à partir d'eau salée.
On considère que les propriétés de l'eau et de l'eau salée sont les mêmes.
Bien que possédant la correction de l'exercice, je ne comprends pas la question a. J'aurais donc besoin d'un peu d'aide svp.
J'ai fait : m4h4 = m5h5+m5h5
or m4=m1 ; m5=m1-m7 ; m6=m7
donc
J'ai déterminé h5 et h6 grâce à des tables (en 5 on a du liquide saturé et en 6 de la vapeur saturée).
Mais impossible de trouver h4. Dans la correction ils mettent qu'on est en présence de liquide saturé mais pourquoi ??
Merci d'avance 
Bonjour
Impossible de t'aider dans de telles conditions ! Il faudrait l'énoncé de l'exercice et un scan des schémas qui l'accompagnent !
On y voit effectivement beaucoup plus clair !
Si je comprends bien, l'état 4 correspond à de l'eau liquide à 150°C.
Vérifie les conventions de tes tables thermodynamiques mais, le plus souvent, l'état d'enthalpie massique nulle est choisi arbitrairement comme l'état de l'eau liquide seule à la température du point triple : 0,01°C.
En considérant comme constante la capacité thermique massique isobare de l'eau liquide :
cp=4,18kJ/kg , on peut considérer que l'enthalpie massique de l'eau liquide seule à la température t (°C) vaut : h=cp.t ;
Ici : h4=4,18.150=627kJ/kg
Merci pour votre réponse.
J'ai bien ici de l'eau liquide mais elle n'est pas pure (eau salée). Etant donné que l'on considère que les propriétés sont les mêmes, votre résultat serait surement considéré comme correct. Dans la correction, il est marqué que je suis censée trouvé est 632.4 kJ/kg.
Je trouve ce résultat lorsque je regarde dans les tables à Tsat=150°C => hfluide=632.4 kJ/kg.
Mais pourquoi le liquide en entrée est-il saturé ?
Pour répondre rigoureusement, il faudrait connaître P4. Si P4=PS(T4) : pression de vapeur saturante à 150°C égale à 476kPa, alors le liquide est saturant. Si P4>PS(T4) alors le liquide n'est pas saturant.
La dernière pression indiquée en amont est P2=700kPa et aucun détendeur n'est placé entre l'état 2 et l'état 4. Même en tenant compte des chutes de pression dans les canalisations, il est à peu près certain que P4>PS(T4).
Cela dit, l'écart relatif entre les deux valeurs n'est que de 0,8%, écart relatif faible devant les incertitudes liées aux déterminations graphiques. Dans ces conditions, plutôt que de fournir la valeur du cp de l'eau liquide, certains auteurs préfèrent poser :
hliq h' à la même température.
h' à la même température.
J'aurais aussi pu ajouter à mon message précédent, que, si, très probablement, l'eau liquide n'est pas saturée, la valeur que j'ai fournie est une valeur approchée : la capacité thermique massique isobare de l'eau n'est pas tout à fait constante : elle varie faiblement en fonction de la température autour de la valeur moyenne 4,18kJ.K-1kg-1 (oui : j'ai oublié le K-1 dans mon message précédent !). Pour être rigoureux, j'aurais dû écrire, pour t=150°C :
Pour conclure, dans le cas d'un liquide non saturant :
1° : si l'énoncé fournit des renseignement sur cp, utiliser le raisonnement de mes messages précédents ;
2° : en absence de renseignements sur cp, poser hliq h' à la même température.
h' à la même température.
On a toutes les données à notre disposition (dont la valeur de Cp et la fonction cp(T)). La correction doit en effet faire selon votre 2ème méthode et approximer que hliq=h. Je voulais être bien sure qu'il n'y avait pas de convention particulière sur l'évaporateur ! Merci d'avoir pris le temps de m'expliquer