Inscription / Connexion Nouveau Sujet
Entropie : Variation d'entropie
Bonjour , je suis complétement bloqué sur la correction d'un exercice je ne comprend pas.
Un kilogramme d'eau à T1=20 degré est mis en contact avec un thermostat à la temperature T0=80° . On donne Ceau = 4,18 J.g-1.K-1
1) Determiner la variation d'entropie de l'eau et du thermostat. Donner l'entropie échangée par l'eau et l'entropie crée.
2) On recommence en maintenant d'abord l'eau en contact avec un thermostat a 50°C puis avec le thermostat à 80°C. Répondre aux même question.
Donc pour la question numéro 1  seau=
seau= 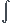 de I a F
de I a F  Q = m Ceau dt (formule de la chaleur pour un solide) je trouve quand je fais l'application numérique 710K.J-1 tandis que dans la correction c'est 778 KJ-1 Je suis perdu helppp me please
Q = m Ceau dt (formule de la chaleur pour un solide) je trouve quand je fais l'application numérique 710K.J-1 tandis que dans la correction c'est 778 KJ-1 Je suis perdu helppp me please 
Oui pardon je me suis mal exprimé donc  seau=
seau= 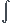
 Q/T or comme je l'ai mis en haut
Q/T or comme je l'ai mis en haut  Q = m Ceau dt . Quand je fais le calcul je trouve 710 K.J-1 Quand je calul le
Q = m Ceau dt . Quand je fais le calcul je trouve 710 K.J-1 Quand je calul le  Q a apar et 779 quand je fais le calcul avec l'intégrale de la facon suivante :
Q a apar et 779 quand je fais le calcul avec l'intégrale de la facon suivante :
 Seau=
Seau= 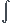 m Ceau dt = mCeau ln ( T0/T1)
m Ceau dt = mCeau ln ( T0/T1)
D'aprés la correction c'est cette deuxieme méthode qu'il faut utilisé mais pourquoi pas l'autre ?! je sais pas si je me fais comprendre ..
il n'y a qu'une façon de calculer la variation d'entropie de l'eau passant de Ti à Tf :
dS éch = m Cp dT / T
 S =
S = 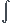 Ti Tf m Cp dT / T
Ti Tf m Cp dT / T
= m Cp 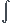 Ti Tf dT / T (si on suppose Cp constant)
Ti Tf dT / T (si on suppose Cp constant)
= m Cp (ln (Tf) - ln (Ti))
= m Cp ln (Tf/Ti)
Quand je fais le calcul je trouve 710 K.J-1 Quand je calcule Q à part
tu peux calculer Q mais tu ne peux pas en déduire
 S
S Merci drep , euh je suis d'accord avec toi mais pourquoi quand je le calcule à part Q cela ne marche pas d'autant plus que pour la deuxième partit de la question il utilise cette méthode. pour calculer  thermostat.
thermostat.
 thermostat= ( m Ceau (T0-T)) / T0 et la on trouve 710 K.J-1 dans ce calcule ci on a pas utliser l'intégrale ainsi que le ln je ne comprend pas pourquoi ? a quel moment on peut faire le calcul de cette manière la ou d'une autre ?
thermostat= ( m Ceau (T0-T)) / T0 et la on trouve 710 K.J-1 dans ce calcule ci on a pas utliser l'intégrale ainsi que le ln je ne comprend pas pourquoi ? a quel moment on peut faire le calcul de cette manière la ou d'une autre ?
Pourquoi je ne peut pas déduire  S si je calcule Q ? etant donnée que
S si je calcule Q ? etant donnée que  S=
S= 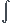
 Q/T = 1/T
Q/T = 1/T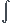
 Q= Q/T je ne vois pas pourquoi on ne pourrai pas faire comme cela pour la première partit de la question sachant qu'ils ont fait cela pour la deuxième partit avec
Q= Q/T je ne vois pas pourquoi on ne pourrai pas faire comme cela pour la première partit de la question sachant qu'ils ont fait cela pour la deuxième partit avec  thermostat , je ne sais pas si tu vois ce que je veut dire ...
thermostat , je ne sais pas si tu vois ce que je veut dire ...
tu mélanges deux transformations différentes:
a) l'eau se réchauffe et passe de 20 à 80°C: dans cette transformation, T varie
tu n'a pas le droit d'écrire: 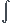 (
( Q/T) = 1/T
Q/T) = 1/T 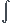
 Q car T n'est pas une constante
Q car T n'est pas une constante
b) le thermostat réchauffe l'eau (en restant à une température constante Tf)
là tu peux écrire: 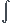 (
( Q/Tf) = 1/Tf
Q/Tf) = 1/Tf 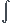
 Q = Q/Tf
Q = Q/Tf
car T = Tf durant toute la transformation, donc 1/Tf est une constante que l'on peut "sortir" de l'intégrale
Yes tout à fait , effectivement sa parait logique , je n'avais pas fais attention merci beaucoup Krinn
effectivement sa parait logique , je n'avais pas fais attention merci beaucoup Krinn  , j'aurai d'autres questions si tu n'est pas pressé ?! Pour trouver l'entropie créee il me faut l'entropie échangée je ne sais pas à quoi cela correspond?!
, j'aurai d'autres questions si tu n'est pas pressé ?! Pour trouver l'entropie créee il me faut l'entropie échangée je ne sais pas à quoi cela correspond?!
On a  seau= Se + Sc , Que vaut Se dans la correction il est écrit que Se= -
seau= Se + Sc , Que vaut Se dans la correction il est écrit que Se= - thermostat = 710 J.K-1 pourquoi donc ..
thermostat = 710 J.K-1 pourquoi donc ..
Entropie échangée par l'eau serait égale a la variation d'entropie du thermostat?
par définition: si un système échange avec l'extérieur la quantité de chaleur  Q à une température Ts (température de la surface d'échange),
Q à une température Ts (température de la surface d'échange),
dSe =  Q / Ts
Q / Ts
donc ici: Se (eau) = Q/Tf = m Cp (Tf-Ti) / Tf (je suppose qu'on attend que l'eau atteigne la température du thermostat)
comme tu as calculé  Sth tu pourras vérifier que:
Sth tu pourras vérifier que:
Se = -  Sth
Sth
sauf erreur





