Inscription / Connexion Nouveau Sujet
Entropie et Transformation d'un gaz parfait
Bonjour
j'ai quelques soucis sur des exos de thermodynamique dont celui ci:
On considère un système constitué d'une mole de gaz parfait dans un état A, caractérisé par TA= 400K, PA= 1 atm. Ce gaz est soumis aux trois transformations suivantes:
1- Transformation adiabatiqye réversible jusqu'à un état B tel que TB= 450 K
2- refroidissement isochore (V=cst) au cours duquel le gaz est au contact d'une source froide de température constante égale à TC
3- transformation isobare qui conduit le gaz à l'état A. Au cours de cette transformation, il échange de la chaleur avec une source de température constante TA.
a) tracer le cycle sur un diagramme P, V.
premièrement, je n'arrive pas à tracer le diagramme. Celui que j'obtiens est de la forme du graphe que j'ai attaché à l'exo, en bas du post. mais il y a une isobare, donc il faudrait une horizontale, non? car là, ma transformation de C vers A correspond + à une isotherme si je ne me trompe pas
b) calculer l'énergie transférée:
-sous forme de travail au cours de chacune des tranformations au cours du cycle ABCA
-sous forme de chaleur au cours de chacune des transformations et au cours du cycble ABCA
en déduire les variations d'énergie et d'enthalipe au cours du cycle ABCA, conclure.
comment trouver ces énergies sans travailler sur le cycle lui même? j'obtiens:
travail réversible de A vers B:
PAVA= nARTA d'où V1 = 0.333
PBVB=nARTB d'où VB = 0.037
soit 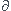 W= -Pext dV
W= -Pext dV
d'où W = - Pext 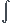 dV = - Pext (Vf-Vi) = -0.04 J.... et là c'est négatif et ça m'étonne...
dV = - Pext (Vf-Vi) = -0.04 J.... et là c'est négatif et ça m'étonne...
ensuite 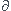 Q= nCpdT (le Cp est donné est est = 29,26 J/k/mol)
Q= nCpdT (le Cp est donné est est = 29,26 J/k/mol)
mais voilà après ça je bloque!!
c)calculer la variation d'entropie ainsi que l'entropie créee au cours de ce cycle ABCA.
je connais les formules mais je ne parviens pas à appliquer...
s'il vous plait, aidez moi!
merci d'avance.
Es-tu sûr du sens de parcours de ton cycle?
Reprends la première transformation et déduis en le sens de variation de et
entre A et B.
Pour une transformation adiabatique, on a la relation:
avec
Tu peux en déduire que le sens de variation de est opposé à celui de
dans une transformation adiabatique. Schéma à revoir...
Par ailleurs:
.
On en déduit donc que
...
Par ailleurs:
on en déduit donc que
je suis daccord on a une adiabatique réversible donc :
cependant je ne comprends pas l'utilisation de
pour trouver le travail, puis je utiliser la relation
de même, je suppose que je dois déterminer la température
en utilisant
je nage complètement, s'il vous plait aidez moi un peu plus...
Puisque l'on te donne directement et
et que , comme je te l'indique, la variation d'énergie interne correspond directement au travail des forces de pression pour une transformation adiabatique:
Pour la suite, étant donné la nature des transformations, ne peux-tu pas déduire et
directement de
et
?
Je sais que ce genre de problème met un jeu un grand nombre d'équations mais il ne faut surtout pas perdre de vue ce que l'on cherche.
Pour une transformation isochore, c'est la valeur du travail des forces de pression qui est facile à déduire.
En partant de , on déduit donc facilement la chaleur échangée durant la transformation
.
Et concernant la dernière transformation , le calcul du travail est évidemment simplifié du fait que
est constant.
Connaissant la variation de l'énergie interne du gaz, on en déduit aussi facilement la chaleur échangée entre les états C et A.
d'accord...merci beaucoup, je crois avoir les idées plus claires désormais. si je rencontre toujours des difficultés, je reviendrais sur mon post.
je trouve
après, pour calculer , étant donné que
est constant, je fais juste
non?
pourpour déterminer je ne peux pas faire la même chose, vu que je n'ai pas la température de C... donc je dois la chercher? mais jai essayé avec
mais comme
je retrouve la même température donc ce n'est pas possible vu qu'on a un refroidissement....
c'est la première fois que je fais un tel exercice (à vrai dire le premier de mon année, j'essaye de le travailler de mon côté avant le TD mais le résultat n'est pas fameux hélas....)
pourriez vous m'apporter encore un peu d'aide, s'il vous plait?
puis le travail sur le cycle est tout bonnement la somme des différents travails bien entendu....
pour la variation d'énergie interne ça coule de source après, ainsi que pour l'entropie et enthalpie.
il faudrait juste que vous m'aidiez pour le travail et la chaleur, s'il vous plaît, je désirerais vraiment comprendre et mieux m'en sortir.
Pour le calcul de : que signifie une transformation "isochore"?
De même, pour la transformation entre C et A, que signifie "isobare"? Qu'en déduit-on pour ?
Avant d'utiliser des formules dans tous les sens, il faut commencer par voir ce que l'énoncé nous donne comme informations...
Et as-tu corrigé ton schéma?
isochore = volume constant... ah oui donc forcément je n'ai pas à me compliquer la vie en calculs...le volume est le même! dc que je peux calculer si je ne me trompe pas.
et donc idem
pour le schéma, je retombe sur le premier que j'ai fait, mais de circulation inverse....
Non, le schéma, ce n'est toujours pas ça ...
Pars de A. Et tiens de compte de la remarque que je t'avais faite à 13h39 hier...
En revanche, pour , puisque le travail des force de pression est nul on a égalité entre la chaleur échangée et la variation d'énergie interne, qui ne dépend que de la température. La connaissance de
est donc en effet suffisante.
A rien? Je croyais qu'on arrivait au bout de l'exercice...
Qu'est-ce qui ne va pas?
On part de et une transformation adiabatique nous emmène à l'état
.
Cette transformation est telle qu'en tout point on vérifie
On peut aussi dire:
d'où et
On doit le retrouver sur le schéma.
en fait je n'avais pas du tout envisagé un cycle fait dans ce sens!!! voilà pourquoi je bloquais!!!! (en supposant que cette fois il est correct ^^)
il ne me manque plus que la chaleur et le travail de B vers C et c'est tout bon!!!!!
merci beaucoup!!!!!!






