Inscription / Connexion Nouveau Sujet
Energie
Bonjour à tous, voilà j'aimerai que vous m'aidiez pour cet exercice s'il vous plait car j'ai du mal à y trouver les réponses. Merci <3
1) qu'est ce qu'un sel et un alcalin ? justifier alors les appellations "piles salines" et "piles alcalines".
2)quelle est la nature des électrolytes de ces piles ?
3) rechercher les caractéristiques des piles alcalines et salines et leurs principales utilisations ?
4) pourquoi faut il recycler ces piles ?
5a) quels sont les réactifs utilisés dans les piles à combustibles de la navette spatiale ?
b) en considérant les réactions d'obtention du combustible utilisé, ces piles sont-elles écologiques ?
6) pourquoi alimenter des voitures par des piles à combustibles ? quels sont les principaux problèmes rencontrés ?
7) citer quelques appareils utilisant des accumulateurs, justifier que ces derniers remplacent de + en + souvent les piles.
8) qu'est ce qu'une pile rechargeable ?
9) une directive européenne interdit la commercialisation d'accumulateurs au cadmium. pourquoi ?
10a) rechercher les caractéristiques d'une batterie d'accumulateurs au plomb.
b) rechercher les caractéristiques des accumulateurs utilisés dans les véhicules électriques.
c) pourquoi n'utilise t'on pas des accumulateurs au plomb dans les véhicules électriques ?
d)ces différents accumulateurs doivent ils être recyclés ? pourquoi ?
Merci à tous de votre gentillesse et j'espère que vous pourriez m'aider pour ces différents questions car toutes mes recherches n'ont aboutis à rien du tout <3
Bien sûr, je ne veux pas que vous me fassiez l'exercice à ma place mais que vous m'aidiez.. qu'il y est des interactions entre nous, comme si on était dans la même pièce et qu'on le faisait ensemble quoi
Merci encore de votre aide.. et est ce que lorsque vous me direz " la réponse " pour telle ou telle question.. pourriez vous préciser ( argumenter ) pourquoi vous avez dit ça ?
Bonjour à tous, voilà j'aimerai que vous m'aidiez pour cet exercice s'il vous plait car j'ai du mal à y trouver les réponses. Merci <3
1) qu'est ce qu'un sel et un alcalin ? justifier alors les appellations "piles salines" et "piles alcalines".
2)quelle est la nature des électrolytes de ces piles ?
3) rechercher les caractéristiques des piles alcalines et salines et leurs principales utilisations ?
4) pourquoi faut il recycler ces piles ?
5a) quels sont les réactifs utilisés dans les piles à combustibles de la navette spatiale ?
b) en considérant les réactions d'obtention du combustible utilisé, ces piles sont-elles écologiques ?
6) pourquoi alimenter des voitures par des piles à combustibles ? quels sont les principaux problèmes rencontrés ?
7) citer quelques appareils utilisant des accumulateurs, justifier que ces derniers remplacent de + en + souvent les piles.
8) qu'est ce qu'une pile rechargeable ?
9) une directive européenne interdit la commercialisation d'accumulateurs au cadmium. pourquoi ?
10a) rechercher les caractéristiques d'une batterie d'accumulateurs au plomb.
b) rechercher les caractéristiques des accumulateurs utilisés dans les véhicules électriques.
c) pourquoi n'utilise t'on pas des accumulateurs au plomb dans les véhicules électriques ?
d)ces différents accumulateurs doivent ils être recyclés ? pourquoi ?
Merci à tous de votre gentillesse et j'espère que vous pourriez m'aider pour ces différents questions car toutes mes recherches n'ont aboutis à rien du tout <3
Bien sûr, je ne veux pas que vous me fassiez l'exercice à ma place mais que vous m'aidiez.. qu'il y est des interactions entre nous, comme si on était dans la même pièce et qu'on le faisait ensemble quoi
Merci encore de votre aide.. et est ce que lorsque vous me direz " la réponse " pour telle ou telle question.. pourriez vous préciser ( argumenter ) pourquoi vous avez dit ça ?
*** message déplacé ***
eh bien là c'est à partir du début ^^ je sais bien que pour certaine questions.. on trouve via la réponse sur google  mais le truc c'est que je ne sais pas si ce qu'ils disent ça va répondre ou pas à la question car tous ce que j'ai vu ça fait des pages et des pages... donc si vous pouviez m'aider pour toute les questions, ça serait géniale
mais le truc c'est que je ne sais pas si ce qu'ils disent ça va répondre ou pas à la question car tous ce que j'ai vu ça fait des pages et des pages... donc si vous pouviez m'aider pour toute les questions, ça serait géniale
non dès la 2) 
aussi revient juste 1 seconde sur l'autre topic et après ici.. j'ai lu ton lien mais il ne répond pas à toute les questions, j'ai l'impression.. donc j'aimerai que tu me dises ce que toi tu répondrais à la question 4c
merci 
2)quelle est la nature des électrolytes de ces piles ?
Il existe deux grandes familles de piles, saline, et alcaline : dans une pile saline, l'électrolyte est un composé salin (chlorure d'ammonium, de zinc, ...) tandis que dans une pile alcaline, l'électrolyte est une solution basique contenant un métal alcalin (lithium, sodium, potassium, ...).
Les piles salines sont toujours basées sur le principe de la pile de Leclanché: une tige de carbone au milieu, une solution saline et une électrode extérieure en zinc. Le carbone est entouré d'un dépolarisateur (le dioxyde de manganèse) pour capter l'hydrogène qui se libère à la surface du carbone. Pendant la décharge, l'électrode en zinc est attaquée, ce qui fait que ces piles peuvent couler quand elles sont vides.
Le terme "pile saline" provient de l'électrolyte utilisé, une solution concentrée de sel (chlorure d'ammonium et de zinc).
Les piles salines classiques sont utilisées de préférence dans les appareils qui ne consomment pas beaucoup de courant. La tension chute rapidement si un gros consommateur est utilisé, mais la tension remonte entre deux utilisations.
Dans certains cas, ce sont les seules piles utilisables, car la tension d'1.2V des accus est trop basse pour entrainer les aiguilles d'une horloge. Dans ces applications spécifiques, il faut obligatoirement une tension d'1.5V.
La capacité d'une pile de format AA est d'environ 1000mAh. Ces piles sont maintenant remplacées par les piles alcalines.
Les piles alcalines utilisent pratiquement le même système, mais les électrodes ont changé de place: au centre il y a une tige de zinc et le carbone et dépolarisant sont placés à l'extérieur. Le boitier est maintenant en tôle d'acier inoxydable. Les deux points faibles sont ainsi éliminés: la plus grande surface extérieure permet un courant plus important, et le zinc placé au centre peut être consommé totalement. La capacité d'une pile alcaline est ainsi nettement plus importante: environ 2500mAh
Comme les piles ne fuient théoriquement plus, on a pu remplacer la solution saline par une solution alcaline, meilleure conductrice (réduction de la résistance interne).
Notez l'existence de piles dites industrielles qui sont en fait de simples piles alcalines vendues sans blister. Ce sont exactement les même piles que tu trouves dans le commerce courant, des mesures électriques (courbe de décharge) le prouvent. Ces piles ont une mention "vente dans le commerce de détail interdite", qui sert surtout à différencier ces piles professionnelles des piles amateur. Un truc commercial qui a du succès, puisque des utilisateurs signalent que ces piles fonctionnent bien mieux, alors qu'il n'y a absolument aucune différence entre ces piles et les piles que tu trouves dans le commerce.
Toutes ces piles (alcalines et surtout salines) ne peuvent pas fournir un courant important (nécessaire dans les appareils photo). L'appareil photo fonctionne un certain nombre de fois et puis se bloque. Les piles ne peuvent pas fournir le courant demandé. Et pourtant, ces piles soit-disant mortes peuvent encore servir un an dans un appareil à faible consommation comme une télécommande
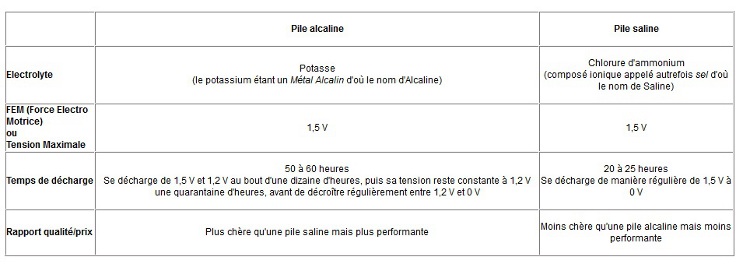
Pour la 4) pourquoi faut il recycler ces piles ?
Je dirais car il sont nocifs mais toi tu dirais quoi ?
ok pas de problèmes merci
je viens de chercher pour la a et la b du 5 je n'ai rien trouvé du tout 
tu peux me dire ce que ta trouvé lolo60 ?
5a) quels sont les réactifs utilisés dans les piles à combustibles de la navette spatiale ?
oxygène et hydrogène
b) en considérant les réactions d'obtention du combustible utilisé, ces piles sont-elles écologiques ?
en considérant les réactions d'obtention du combustible utilisé lesquels?
l'oxygène est présent partout sur terre
l'hydrogène par contre doit être produit
Dans un sens elles sont écologiques, puisque elles ne rejettent que de l'eau
Quelqu'un ?
Je ne trouver rien pour ces 4 questions ^^
10a) rechercher les caractéristiques d'une batterie d'accumulateurs au plomb.
b) rechercher les caractéristiques des accumulateurs utilisés dans les véhicules électriques.
c) pourquoi n'utilise t'on pas des accumulateurs au plomb dans les véhicules électriques ?
d)ces différents accumulateurs doivent ils être recyclés ? pourquoi ?
rechercher les caractéristiques d'une batterie d'accumulateurs au plomb.
Une batterie au plomb est un ensemble d'accumulateurs au plomb-acide disposés en série, réunis dans un même boîtier.
Ces systèmes de stockage de l'électricité sont largement utilisés dans l'industrie et, dans l'équipement des véhicules automobiles.
Caractéristiques techniques
Une batterie au plomb se caractérise essentiellement par :
- La tension nominale qui dépend du nombre d'éléments, la tension nominale U est égale au nombre d'éléments multiplié par 2,1 V
- La capacité de stockage, notée C, qui s'exprime en ampères pendant 1 heure : l'énergie électrique théorique correspondante est C x U, exprimée en Wh. (Notons que la valeur en Ah n'a de valeur que pour une tension ou plutôt une plage de tension. Généralement on considère qu'un accumulateur au plomb est déchargé lorsqu'il atteint la tension de 1.8 V, donc une batterie de 6 éléments ou 12 V est déchargée, lorsqu'elle atteint la tension de 10.8 V).
- Le courant maximal qu'elle peut fournir pendant quelques instants, ou courant de crête en ampères CCA.
Ces valeurs maximales sont donnés par le constructeur pour une batterie neuve et chargée à 100%, elles varient sensiblement en fonction de l'état de charge, se dégradent en fonction du temps ainsi, que de l'usage qui est fait de la batterie.
Performances
La batterie au plomb est celle qui a le plus mauvais rapport masse/énergie (35 Wh/kg) après la batterie Nickel-Fer. Cependant, elle est capable de fournir une grande intensité, utile pour le démarrage électrique des moteurs à combustion interne.
Utilisation
Cette batterie sert à alimenter les composants électriques des véhicules à moteur à explosion, particulièrement le démarreur électrique, alimentée par une dynamo ou un alternateur.
Historiquement, les batteries de voitures ou de motocyclettes faisaient le plus souvent 6 volts (3 éléments). À l'époque moderne, les batteries à 12 volts (6 éléments) sont généralisées sur les voitures et motocyclettes, alors que les véhicules lourds ou militaires utilisent le 24 volts.
Les batteries au plomb servent aussi à alimenter toutes sortes d'engins électriques. Les voitures électriques ont toujours échoué du fait du mauvais rapport masse/énergie des batteries.
source :
Ces batteries peuvent servir à stocker de l'énergie produite par intermittence, comme l'énergie solaire ou éolienne.
c) pourquoi n'utilise t'on pas des accumulateurs au plomb dans les véhicules électriques ?
car les accumulateurs au plomb sont bien plus lourds et imposant que les accumulateurs au lithium ce qui alourdirait le poids du véhicule électrique
d)ces différents accumulateurs doivent ils être recyclés ? pourquoi ?
oui, car ils contiennent des substances néfastes pour l'environnement. De plus, le recyclage de ces accumulateurs permet de récupérer des matières chimiques qui peuvent être réutilisés
b) rechercher les caractéristiques des accumulateurs utilisés dans les véhicules électriques.
La batterie electrique est l'organe clé des voitures électriques. Elle influe directement sur les performance et surtout l'autonomie de l'automobile écologique. Aujourd'hui, les batteries lithium permettent d'améliorer considérablement les caractéristiques techniques des véhicules électriques et rend leurs l'utilisation possible.
Le lithium permet en effet de stocker énormément de charges électriques sous forme d'ions sur les électrodes et de manière très compacte. Le principe de fonctionnement réside sur la circulation des électrons pour générer un courant électrique, comme pour toute autre batterie : les ions lithium, agglutinés sur l'électrode négative en graphite, traversent l'électrolyte (paroi centrale de la batterie), pour se fixer sur l'électrode positive en dioxyde de cobalt.
caractéristiques
La densité massique est de 260 Wh/kg2. Par comparaison, elle contient presque 7 fois plus d'énergie que les batteries au plomb (~40 Wh/kg) à poids égal car la structure en film mince est légère et maximise la surface de stockage utile d'énergie.
Il n'y a pas d'effet mémoire, on n'a donc pas besoin de vider complètement l'accumulateur avant de le recharger.
La durée de vie annoncée des batteries utilisant cette technique est de l'ordre de dix ans.
Cependant, pour un fonctionnement optimal, l'électrolyte a besoin d'être maintenu à une température avoisinant 85 °C.
Avantages
Entièrement solide (pas de risque d'explosion).
Faible auto-décharge.
Inconvénients
Fonctionnement optimal à température élevée.
source:
Pas de polluant majeur dans la composition de l'accumulateur (sauf si utilisation d'oxyde de vanadium).
Merci beaucoup lolo
4) pourquoi faut il recycler ces piles (alcalines et salines )?
j'ai cherché mais aucun document me permettant de dire de façon approfondis la réponse à cette question.. de ce fait, je te demande si toi tu le sais... ( je le sais mais ce n'est en aucun cas argumenter) ainsi je te demande si tu pourrais me dit en précision pourquoi les recycler. merci
également je n'ai rien trouvé
7) citer quelques appareils utilisant des accumulateurs, justifier que ces derniers remplacent de + en + souvent les piles.
9) une directive européenne interdit la commercialisation d'accumulateurs au cadmium. pourquoi ?
j'ai trouve des articles disant qu'ils interdisaient les accumulateurs au cadmium mais non pourquoi
donc j'aimerai que tu m'expliques de façon précise, argumentez(pas un paragraphe non plus^^) mais quelque chose de long qui explique de façon claire la chose 
merci beaucoup Lolo60  <3
<3
En gros j'aimerai de l'aide pour ces 3 questions :
4) pourquoi faut il recycler ces piles (alcalines et salines )?
7) citer quelques appareils utilisant des accumulateurs, justifier que ces derniers remplacent de + en + souvent les piles.
9) une directive européenne interdit la commercialisation d'accumulateurs au cadmium. pourquoi ?
merci beaucoup 
4.Pourquoi et comment recycler les piles ?
Les piles et les accumulateurs contiennent des métaux lourds (mercure, zinc, plomb, cadmium) en grandes quantités. Ces métaux lourds sont connus pour être dangereux pour la santé et pour l'environnement : une pile au mercure jetée dans la nature suffit pour contaminer 1m3 de terre et 1000 m3 d'eau pendant 50 ans !
En raison de la dangerosité des métaux lourds, la santé publique est également concernée par ces pollutions.
Les intoxications au mercure sont possibles par inhalation ou ingestion. Manger des animaux contaminés par le mercure est donc un vecteur d'intoxication. Ce métal est connu depuis l'antiquité pour provoquer des troubles neurologiques : tremblements, difficultés d'élocution
Les autres métaux lourds ont des effets tout aussi effrayants sur le système nerveux, le sang et les reins.
![]()
7) citer quelques appareils utilisant des accumulateurs, justifier que ces derniers remplacent de + en + souvent les piles.
appareil photos, téléphone portable, ordinateur portable, gps,...
Les accumulateurs ont la particularité de pouvoir se recharger
9) une directive européenne interdit la commercialisation d'accumulateurs au cadmium. pourquoi ?
car il fait partie des métaux lourds qui sont des composés toxiques et dangereux


 ) :
) :

