Inscription / Connexion Nouveau Sujet
Donneur ou accepter de liaisons hydrognènes = quand ?
Bonjour à tous !
Cette année, je fais un peu de chimie organique, et je vois notamment quels sont les composés qui s'associent par liaisons hydrogènes, lesquels par autres forces de Van der Walls, s'ils sont donneurs et/ou accepteurs de liaisons hydrogènes...
Or, je galère un peu à tout retenir par coeur !
Existe-t-il une règle générale permettant d'établir si un composé peut former des liaisons hydrogènes ? Si oui, existe-t-il une autre règle pour déterminer s'il est donneur, accepteur ou les deux ?
Merci beaucoup par avance !
Bonne journée 
Bonjour,
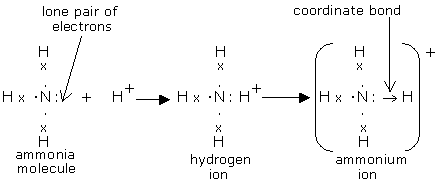
Vous devez examiner la structure de Lewis de vos atomes.
S'il possède un doublet non liant, alors il est donneur (ex : atome d'Azote N, atome d'oxygène O, les halogènes, ...), c'est une base de Lewis (site nucléophile).
S'il possède une case vide (couche incomplète), alors il est accepteur du doublet (ex : ion H+, atome de Magnésium Mg, atome d'aluminium Al, ... ), c'est un acide de Lewis (site électrophile).
Ainsi vous pouvez former l'ion ammonium NH4(+) en partant de l'ammoniac NH3 par liaison de coordination.