Inscription / Connexion Nouveau Sujet
Dilution et facteur de dilution
Bonjour à tous,
J'ai réalisé un TP sur le dosage des anthocyanes sur la groseille et j'aimerai savoir si je ne me suis pas trompée dans mes calculs de dilution.
Je vous mets l'énoncé juste en dessous ainsi que mes réponses.
"Cette méthode utilise deux systèmes tampon : Le chlorure
de potassium à 0,025 M (pH1 = 1,0) et l?acétate de sodium à 0,4 M (pH2 = 4,5).
- Dans une cuve de spectrophotomètre, mélanger 0,4 ml d?extrait avec 3,6 ml de chaque solution
tampon.
- Mesurer l?absorbance à 510nm et 700nm de ces mélanges.
- Déterminer si des dilutions sont nécessaires pour poursuivre les mesures.
- Une fois les bonnes conditions déterminées, réaliser les calculs d?absorbance en triplicat.
L?absorbance qui correspond aux anthocyanes est calculée comme suit :
A = (A510nm ? A700nm) pH 1 ? (A510nm ? A700nm) pH 4.5"
En effet, j'ai du réaliser une dilution pour le pH1 car l'absorbance était trop grande. J'ai donc fais une dilution au demie:
-1mL d'extrait et 1mL d'eau distillée
J'ai donc trouvé une bonne absorbance. Cependant, je ne pense pas que ça soit bon et je n'arrive donc pas à trouver le facteur de dilution. Pouvez-vous m'aider et me dire si ce que j'ai fais est bon et comment trouver le facteur de dilution s'il-vous-plaît.
Je vous remercie d'avance.
***Forum changé***
Bonjour,
Je n'arrive pas à trouver la constante de dégradation k à partir d'un tracé de Ln(A/A0)=Ln. Pouvez-vous m'aider à partir de mon graphique ci-dessous.
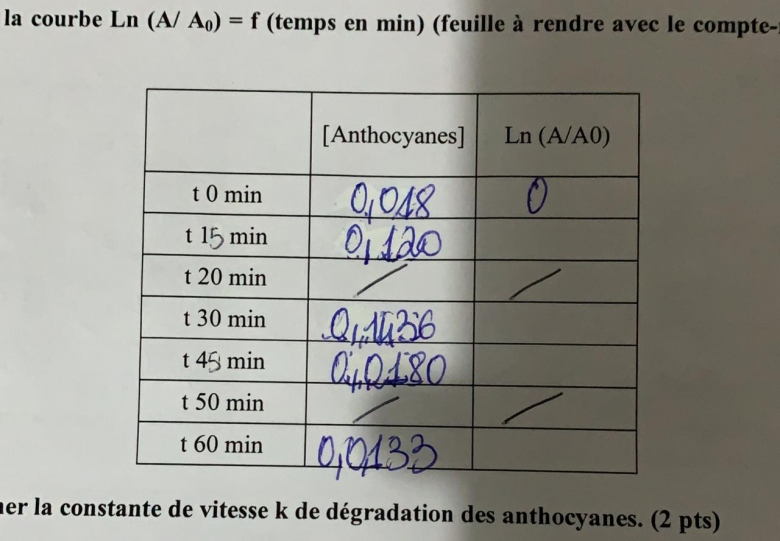
Je connais A mais je ne connais pas A0 donc je n'arrive pas à compléter le tableau Ln (A/A0).
Je vous remercie d'avance.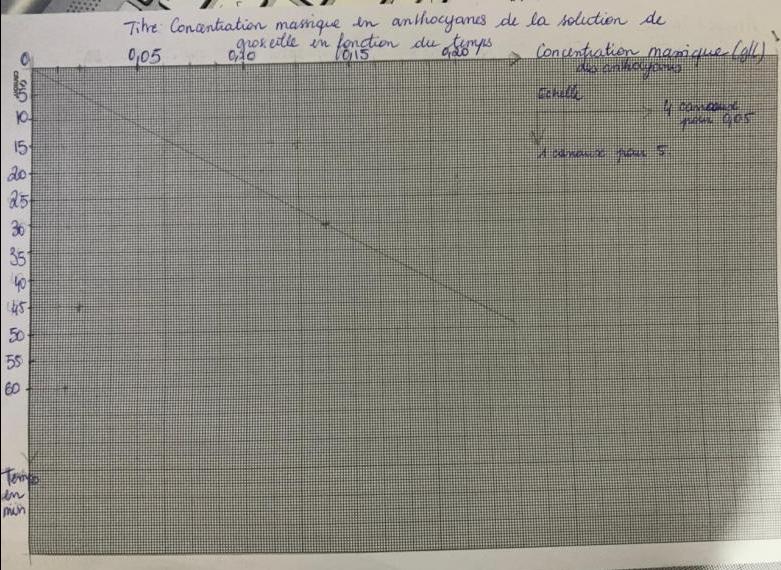
***Forum changé***
*** message déplacé ***
Bonjour,
Découper le même TP en plusieurs sujets = multipost
Ensuite, le fait de ne pas poster un énoncé complet (dans le respect du règlement) rend difficile toute aide :

Bonjour
Les valeurs de [A] figure dans la colonne de gauche de ton tableau (unité à préciser). La valeur [A]o est tout simplement la valeur à t=0 : 0,018.
Par exemple : à t=15min :
ln(A/Ao)=ln(0,12/0,018) 1,90
1,90
Je t'ai indiqué la méthode mais j'ai quelques doutes sur la fiabilité des mesures. Il est questions de dégradation des anthocyanes. La valeur de [A] devrait donc diminuer en fonction du temps.
Bonjour,
Découper le même TP en plusieurs sujets = multipost
[faq]multi[/faq]
Ensuite, le fait de ne pas poster un énoncé complet (dans le respect du règlement) rend difficile toute aide :
[faq]redac[/faq]

Bonjour,
Découper le même TP en plusieurs sujets = multipost
[faq]multi[/faq]
Ensuite, le fait de ne pas poster un énoncé complet (dans le respect du règlement) rend difficile toute aide :
[faq]redac[/faq]

Veuillez m'en excuser je n'avais malheureusement pas bien lu.


 ) :
) :
 remercier la personne
remercier la personne

