Inscription / Connexion Nouveau Sujet
Diagramme énergétique d'un atome de sodium
Bonjour, j'ai fais entièrement un exercice de physique, j'aimerais que vous vérifiez mon travail. 
Voici l'énoncé :
En1868, le français Pierre Janssen et le britannique Norman Lockyer ont découvert en analysant
le spectre de la couronne solaire une raie brillante dans le jaune très proche de celle du
sodium. N. Lockyer a émis l'hypothèse que cette raie était due à un nouvel élément l'hélium
qui sera identifié sur Terre vingt-sept ans plus tard.
Données :
Célérité de la lumière dans le vide : c = 2,998.10 8 m.s- 1
Constante de Planck : h = 6,626.10 - 34 J.s
Longueur d'onde de la raie D du sodium dans le vide : λNa = 589,0 nm.
Longueur d'onde de la raie jaune de l'hélium dans le vide : λHe = 587,6 nm.
1 eV = 1,602.10 - 19J.
Les questions et mes réponses :
1 Le diagramme énergétique de l'atome de sodium montre que l'énergie ne peut prendre que certaines valeurs. Comment qualifie-t-on alors l'énergie ?
Ma rép : L'énergie de l'atome est quantifiée.
2 Comment désigne-t-on le niveau le plus bas E0 sur le diagramme énergétique ?
Ma rep : Le niveau le plus bas sur le diagramme énergétique est le niveau fondamental.
3 Un électron cède une partie de son énergie à un atome de mercure. L'énergie de celui-ci passe du niveau E0 au niveau E1. Comment qualifie-t-on l'état dans lequel se trouve alors l'atome de mercure ?
Ma rep : L'état où se trouve l'atome de mercure est l'état excité.
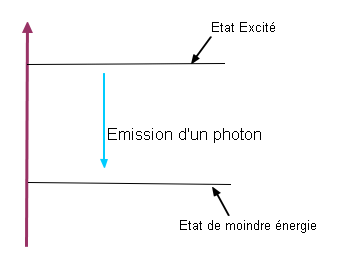
4 Illustrer, en s'aidant d'un schéma de niveaux d'énergie d'un atome, le phénomène d'émission d'un photon (quantum d'énergie lumineuse).
Illustration en fin de message
5 On note E l'énergie du photon émis lors d'une transition énergétique d'un atome. Donner l'expression littérale de E en fonction de la longueur d'onde λ de la radiation lumineuse émise dans le vide, de la constante de Planck h et de la célérité de la lumière dans le vide c.
Ma rep : Expression littérale de E:
E= hc/ λ
6 On s'intéresse à la raie D du sodium
a) Calculer la valeur de E, en électronvolts, pour le rayonnement correspondant à la raie D du sodium.
Ma rep :
Valeur de E en électronvolts, pour le rayonnement correspondant à la raie D du sodium :
E = 6,626 10-34* 2,998 108 / (589,0 10-9 )= [6,626 *2,998 / 589]* 10-17 J
Diviser par 1,602 10-19 pour obtenir l'énergie en eV
E = [6,626 *2,998 / (1,602*589]* 102
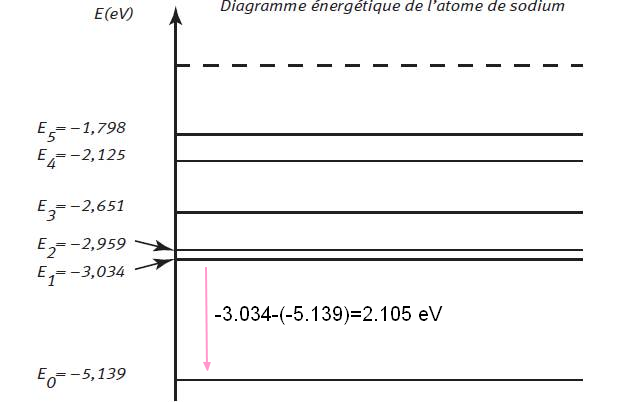
E= 2,105 eV
b) Déterminer, en s'aidant du diagramme, à quelle transition correspond cette émission.
Diagramme en fin de message
7 L'énergie du photon correspondant à l'émission de la raie jaune de l'hélium (de longueur d'onde λHe) est égale à 2,110 eV. En s'aidant du diagramme, justifier que cette émission ne peut pas être attribuée au sodium.
Ma rep : Cette émission ne peut pas être attribuée au sodium : 2,110 eV ne correspond à la différence d'énergie entre deux niveaux d'énergie de l'atome de sodium.
Merci d'avance pour votre correction.
Illustration et diagramme :
Un modérateur peut-il supprimer ce message, je n'ai plus besoin d'aide, s'il vous plait, merci d'avance. 


