Inscription / Connexion Nouveau Sujet
Construction de pile
Bonjour,
J'ai besoin d'aide pour résoudre cet exercice:
On construit une pile sur la base des couples rédox ( à 25 °C)
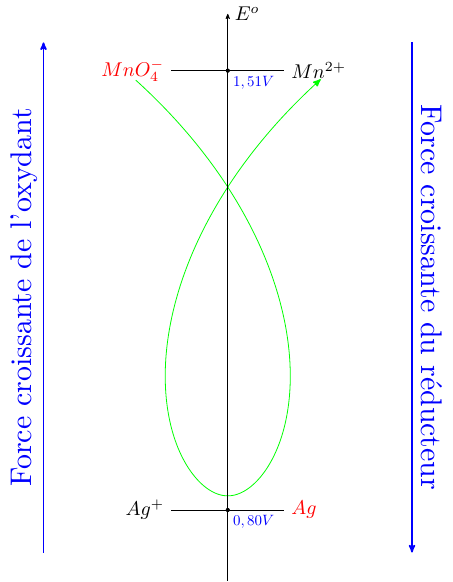
MnO4-/Mn2+ et Ag+/Ag
Je dispose des concentrations initiales en MnO4-, Mn 2+ et Ag +, je sais aussi que le pH=4,45 et que les volumes de solution à l'anode et à la cathode sont de 30,0 mL
a)Quelle est la réaction globale qui actionne la pile
b)Calculez la force électromotrice de la pile à l'instant initial.
c)On ajoute 15,0 mL d'une solution de chlorure de sodium, NaCl, 0,855 mol/L dans le compartiment qui contient les ions Ag+de la pile décrite ci-dessus. On observe la formation d'un précipité. Calculez la force électromotrice de la pile après ajout du NaCl.
Je dispose aussi des potentiels standards d'oxydo-réduction
J'ai pas mal de lacunes théoriques les piles électrochimiques,
est ce que E°(Ag+/Ag) = 0,8 V veut dire que l'oxydation d'Ag par un oxydant quelconque va placer l'électron libéré sous un potentiel de 0,8V et va donc être soumis à une force électromotrice qui va l'obliger à circuler dans un fil pour se diriger vers la cathode ?
pour répondre à la A j'ai trouvé sur internet la règle du gamma qui dit que
Ox2 + Red1 → Red2 + Ox1 avec E°2 > E°1
a) avec la règle du gamma : Mn2+ + 4Ag + H2O ---> 4Ag+ + MnO4- + 2H+
est ce bien ça ? plus le E° est grand plus la spontanéité de la réaction est grande, c'est bien ça la règle du gamma ?
b) la force électromotrice totale = E°(Ag+/Ag) - E°(MnO4-/Mn2+)
Merci d'avance à celui ou celle qui m'aidera
Bonjour
Attention au sens de la réaction : la règle du gamma conduit à faire réagir l'oxydant le plus fort sur le réducteur le plus fort. As-tu classé tes deux couples par ordre de potentiels standard croissants ? Tu dois aussi écrire les deux demies équations correspondant aux deux couples. Cela va te permettre d'équilibrer correctement l'équation bilan et aussi, en déterminant les deux potentiels de Nernst, d'obtenir la fém initiale de la pile.
Je te laisse réfléchir...
Merci Vanoise
Donc à l'aide de ton schéma:
Comportement Anodique (oxydation) : Ag(solide) ---> Ag+(liquide) + e-
Comportement Cathodique (réduction) : MnO4-(liquide) + (???) + e- ---> Mn(solide)
Je ne sais pas quoi additionner à MnO4 pour obtenir mon comportement cathodique, je me doute que ça sera H20 ou OH- puisque ce sont les deux principales molécules présentes
En faite la règle du gamma provient juste du fait que l'oxydant le plus fort va d'office être utilisé pour la réduction et le réducteur le plus fort pour l'oxydation ???
Sinon tu saurais me confirmer qqchose que je ne comprends pas très bien et pour laquelle je en trouve pas d'explications claires :
est ce que E°(Ag+/Ag) = 0,8 V veut dire que l'oxydation d'Ag (qui est donc spontanée ?) va placer l'électron libéré sous un potentiel de 0,8V et va donc être repoussé par la force de coulomb due principalement aux électrons de valence de Ag ? et c'est comme ça que marche une pile ?
Puisque la notion de nombre d'oxydation n'est sans doute pas à ton programme, je te rappelle la méthode vue dans l'enseignement secondaire pour équilibrer une demie équation, ici : celle correspondant à la réduction des ions permanganate en ions manganèse.
1° étape : conservation de l'élément principal : ici l'élément Mn ; 1 à droite et un à gauche ;
2° étape : conservation de l'élément oxygène en ajoutant des molécules d'eau ;
3° étape : conservation de l'élément hydrogène en ajoutant des ions H+
4° étape : conservation des charges électriques en ajoutant des électrons.
En faite la règle du gamma provient juste du fait que l'oxydant le plus fort va d'office être utilisé pour la réduction et le réducteur le plus fort pour l'oxydation ???
oui.
Le potentiel standard est la différence de potentiel entre la demie pile correspondant au couple étudié (par exemple la demie pile correspondant à Ag+/Ag) et la demie pile standard à hydrogène correspondant au couple H+/H2
Il te faut absolument étudier un cours précis sur l'oxydo réduction.
les bases :
niveau un peu plus élevé :
En utilisant les étapes :
Comportement Cathodique (réduction):
1) MnO4- ---> Mn2+
2 et 3) MnO4- + 8H+ ---> Mn2+ + 4H2O
4) MnO4- + 8H+ + 5e- ---> Mn2+ + 4H2O
c'est bien ça ? et donc la réaction globale serait :
5Ag + MnO4- + 8H+ ---> Mn2+ + 4H2O + 5Ag+ ?
J'ai lu les deux cours mais ils ressemblent beaucoup à ce que j'ai déjà étudié, j'aimerais comprendre ce qui fait se déplacer l'électron à travers le fil en cuivre, en cherchant sur internet voici ce que je pense être le fonctionnement d'une pile :
Le potentiel standard serait la différence de potentiel entre l'anode et la cathode, d'une pile dans laquelle aurait lieu la réduction d'H+ à la cathode, et l'oxydation d'un réducteur quelconque à la cathode, c-à-d (je pense) que les protons H+ vont attirer les électrons de valence du réducteur quelconque et l'oxyder ce qui va provoquer le déplacement des électrons, mais alors si c'est vraiment ça pourquoi aurait t'on des potentiels standards négatifs ?
Tous ça dans les conditions standards : P = 1 atm, molarité = 1, t° = 25 °
OK pour l'équation bilan. Il te faut ensuite déterminer les potentiels de Nernst des deux demies piles.
j'aimerais comprendre ce qui fait se déplacer l'électron à travers le fil en cuivre
Si tu plonges une tige d'argent dans une solution acide de permanganate de potassium, la réaction dont tu viens d'écrire l'équation bilan se déroule spontanément avec dégagement d'énergie thermique. L'argent perd spontanément des électrons en s'oxydant, ces électrons étant absorbés par les ions permanganates lors de leur réduction. Toute l'astuce de la pile consiste à placer l'oxydant et le réducteur dans deux récipients différents que l'on relie par un circuit électrique, sans oublier bien sûr de fermer le circuit par un pont salin. Le transfert d'électrons s'effectue alors à travers le circuit électrique, ce qui permet de récupérer sous forme d'énergie électrique une partie de l'énergie fournie par la réaction chimique. Tout cela est heureusement cohérent avec la notion de potentiel. La formule de Nernst permet de démontrer que les potentiels des deux demies piles sont différents. Le sens conventionnel du courant dans le circuit électrique extérieur à la pile va de la demie pile au potentiel le plus élevée vers la demie pile au potentiel le plus faible, les électrons circulant en sens inverse.
Petite remarque : depuis 1882, la pression standard vaut 105Pa et non 1,013.105Pa=1atm.
Il existe des conditions standard à n'importe quelle température. Il n'existe donc pas de température standard. Les tables thermodynamiques fournissent souvent les valeurs standard à 25°C mais cela ne veut pas dire que 25°C est la température standard !
Yes super !
Merci pour ton exemple mais de nouveau comme dans la plupart des cours que j'ai lus, on explique le voyage de l'électron à partir des notions d'oxydants et réducteurs mais on parle moins de l'attraction électrique, si l'électron voyage d'une molécule à une autre c'est à cause de la force de coulomb mais comment ça marche ?
Est ce que, plus un atome possède une couche complète d'électrons de valence, plus il va se faire réduire facilement (à cause du fait qu'il possède plus de protons) par rapport à un atome de la première colonne, qui a plus de mal à garder son électron de valence (car moins de protons) et pourrait se faire oxyder très facilement ?
Si c'est bien le cas alors H être l'atome qui se fait oxyder le plus facilement de tout l'univers !
Ce que je viens de dire est juste ?
Sinon b):
Par la réaction globale de ma pile, la différence de potentiel (dans les conditions standards) de la réaction est la somme entre le potentiel standard de l'oxydation d'Ag et la réduction de MnO4
$\delta$E° = -0,8 + 1,51 = 0,71 volt
Dans notre cas on n'est pas face à des conditions standards car la molarité initiales est différente de 1, on peut utiliser l'équation de Nernst :
-n.F.$\delta$E = $\delta$G
<=> $\delta$E = $\delta$E° - (R.T)/(n.f) ln(Q)
Où Q est le quotient réactionnel à l'instant où on commence la réaction chimique de la pile
Deux remarques rapides.
1° : il existent des potentiels standard négatifs. Par exemple celui du couple Zn2+/Zn ; le dihydrogène n'est donc pas le réducteur le plus fort de l'univers ! Les métaux usuels (pas les métaux précieux) sont plus réducteurs que le dihydrogène.
2° calculer la fém standard à partir des potentiels standard puis calculer la fém en fonction de la fém standard et du quotient de réaction est une méthode possible. Néanmoins, j'ai remarqué qu'elle engendre très souvent des erreurs de signe. Il me semble plus sûr de calculer séparément chaque potentiel de demie pile à partir de la formule de Nernst puis de considérer que la fém réelle est la différence de ces deux potentiels.