Inscription / Connexion Nouveau Sujet
Combustion de Lavoisiers
Bonjour, j'ai un devoir a rendre en physiques chimie mais je reste bloquer sur un exercice le voici :
Antoine Lavoisiers, chimiste .... Constate que lors un combustion la masse des métaux augmente.Il en conclut qu'une partie de l'air s'associe au métal en court de transformation
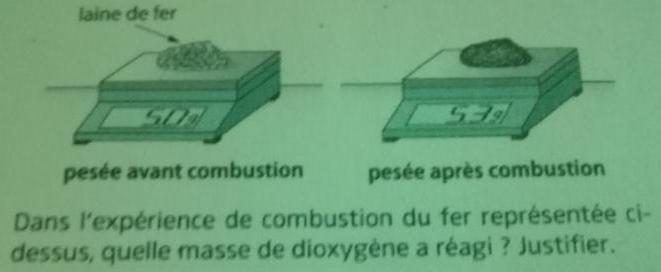
Question : Dans l'expérience de combustion du fer représenté ci-dessus, quelle masse de d'oxygène a réagi ?Justifier
Merci, de votre aide
Bonsoir Maxoulin :
La combustion du fer dans l'air ou le dioxygène est une réaction chimique entre le fer et le dioxygène. Cette réaction dégage de l'énergie : on dit qu'elle est exoénergétique. Le produit de cette réaction est un oxyde de fer. Formule des réactifs : Fe pour le fer et O2 pour le dioxygène.
3 Fe + 2 O2 ======> Fe3O4
Bonnes salutations .
Rebonsoir : ( je m'excuse , j'ai oublié la fin du problème ? )
Masse atomique du fer = 55,85 .
Masse moléculaire du dioxygène = 32 .
Masse moléculaire de Fe3O4 = 231,55 .
3 Fe + 2 O2 ======> Fe3O4
Dans l'équation , 3 moles de Fer ( 3 x 55,85 = 167,55g ) demandent 2 moles de
dioxygène ( 2 x 32 = 64g ) , pour donner 1 mole de Fe3O4 soit 231,55g .
( Il y a une erreur sur la présentation ? 50g de fer ne peux pas donner 53g d'oxyde ? )


