Inscription / Connexion Nouveau Sujet
Chimie organique
Bonjour a tous j'ai une question concernant cette exercice pourriez-vous m'aider s'il vous
D'après la technique de séparation chimique, on aimerait séparer un mélange d'acide benzoïque et de phénol. Comment allez-vous procéder pour récupérer dans un bécher, l'acide benzoïque et dans un autre bécher, le phénol ? Expliquez cette technique sur base d'équations chimiques.
Je n'arrive pas à résoudre cette exercice quelqu'un peut m'aider s'il vous plaît.
Merci d'avance.
Bonjour
J'imagine les deux produits mélangés dans un solvant organique commun. Une méthode possible consiste à faire réagir le mélange sur une solution aqueuse contenant une base de pKa compris entre les pKa des deux produits à séparer.
Je te laisse rechercher les pKa et trouver une base possible. Cette base va transformer l'acide benzoïque de façon quasi totale en sa base conjuguée qui, elle, est très soluble dans l'eau. Après décantation, on obtient le phénol dans la phase organique et les ions benzoate dans la phase aqueuse. On revient alors à l'acide benzoïque en acidifiant la solution aqueuse.
Je te laisse mettre tout cela au clair...
Compte tenu de mon premier message, commence par répertorier les 3 couples acide/base susceptibles d'intervenir avec les pKa correspondants. Tu y verras plus clair ensuite.
Cela devrait t'aider. Les espèces susceptibles de réagir sont écrites en rouge. Tu peutx écrire les équations bilan puis calculer les constantes d'équilibre.
Il te faudra montrer ensuite que les ions hydrogénocarbonate réagissent de façon quasi totale sur l'acide benzoïque et ne réagissent quasiment pas sur le phénol.
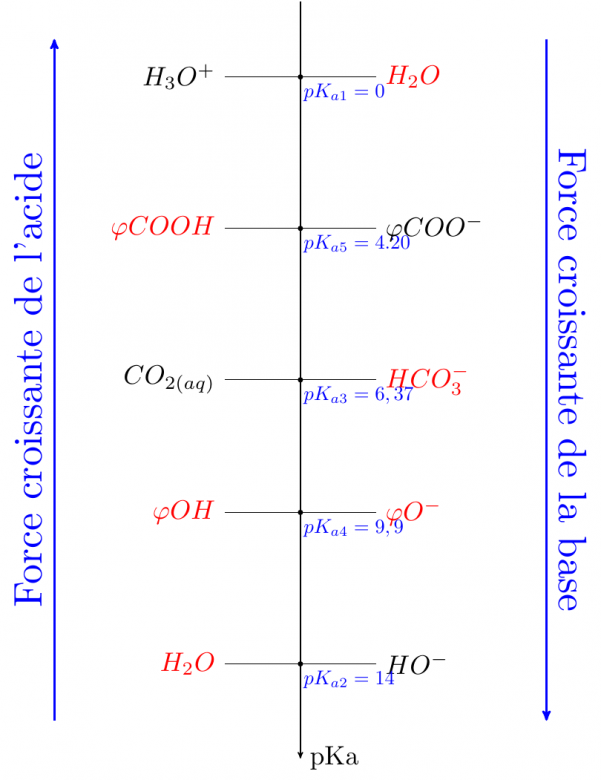

 O- devrait être en noir... Cela ne va pas changer grand chose au raisonnement...
O- devrait être en noir... Cela ne va pas changer grand chose au raisonnement...
