Inscription / Connexion Nouveau Sujet
chimie molécules
Bonjour pouvez vous m'aider svp ? merci d'avance
On cherche à déterminer la nature d'un ose A, ainsi que la position du pont oxydique établi au sein de la molécule.Le cétose intermédiaire obtenu lors de l'interconversion de cet ose, est le D-tagatose.
1) Quel peut-être la nature de la molécule A?
2)Sachant que cette molécule est un composant du lactose, donner le nom de cet ose.
Tu connais la formule du tagatose? Or on te dit que c'est sa forme D ce qui te donne des indices quand à la position relative des groupements alcools par rapport à la chaîne linéaire.
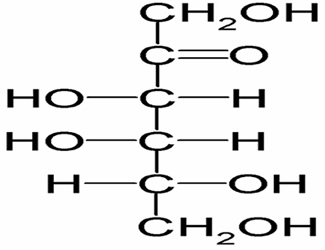
ba le D-tagatose est voir ci dessous, cependant si je comprend bien quand on dit groupement alcool on parle bien de l'avant dernier OH qui est du côté droit ????
Mais après comment on peut savoir pour la nature de l'ose A ????Merci d'avance de m'éclairer !!!
oui pour le dernier OH de la chaîne linéaire.
Tu sais ce qu'est un pont oxydique et tu sais comment il se forme?
non je ne vois vraiment pas pour le pont oxydique ! Sinon on parle bien du même OH celui qui est au dessus du CH2OH,ne doit t-on pas regarder généralement au niveau du OH du 1 er carbone pour savoir si c'est le Dtagatose ou Ltagatose ?????
Si je comprend bien :
Lorsque le OH du Carbone 1 est vers la droite, nous avons une molécule à nomenclature α.
Lorsque le OH du carbone 1 est vers la gauche, nous avons une molécule à nomenclature β.
Lorsque le OH de l'avant dernier carbone est vers la droite alors c'est D
Lorsque le OH de l'avant dernier carbone est vers la gauche alors c'est L
Cependant pour le 2éme cas pour le cycle furanique (dans le lien que vous me montré)pourquoi le pont oxydique ne se ferme pas entre 2 OH ???? Doit-il seulement commencer entre 2 OH ????
Je ne comprends pas ta dernière question 
Mais oui pour tes interrogations. Tu vois maintenant ce qu'est un pont oxydique?
ba ce que je veux dire c'est es- ce qu'un pont oxydique doit se faire au début obligatoirement entre 2 OH ???
et quand il se ferme même question ?
oui mais pourquoi dans le 2éme cas pour le cycle furanique au niveau du carbone 3 et 5 on a pas 20H mais H et OH ????
=>Le C1 (fonction aldéhyde) peut se lier à un autre carbone de la molécule par l'intermédiaire d'un atome d'O. Il y a formation d'un pont oxydique.
Il existe 2 principales possibilités de cyclisation pour le glucose :
#le pont oxydique se fait entre le C1 et le C5, on obtient un cycle hexagonal. On dit que l'axe est sous
forme pyranose.
Par exemple le glucopyranose (glucose sous forme cyclique avec un cycle à 6 côtés)
#le pont oxydique se fait entre le C1 et le C4, on obtient un cycle pentagonal. L'ose est désigné avec le
terme furanose.
Exemple le glucofuranose
Pour les cétoses, c'est le C2 (qui porte la fonction cétone) qui va réagir avec un autre C.
Pour ta question du D et L
=>La représentation de la forme cyclique est appelée représentation de Haworth. Dans cette représentation,
les OH qui étaient situés à droite en représentation de Fischer se retrouvent en dessous du plan du cycle et les
OH qui étaient situés à gauche, au-dessus du plan du cycle. On reconnaît la série D et la série L par rapport à la
position de l'extrémité de la chaîne carbonée.
#si le CH2OH du C6 est situé en haut (au-dessus du cycle) ---> série D
#si le CH2OH est situé en bas ---> série L
Lors de la cyclisation, le C1 devient asymétrique, il y a alors 2 formes isomères qui existent :
#une forme α : lorsque le OH du C1, et le CH2OH du C6 sont en opposition
#une forme β : lorsque le OH du C1 et le CH2OH du C6 sont situés du même coté
Le carbone qui forme le groupement carbonyle dans la structure linéaire est le carbone qui est hydraté lors du phénomène de cyclisation. Ce carbone sera donc le carbone anomérique dans la forme cyclique.
Il s'agira toujours du carbone 1 dans le cas d'un aldose et du carbone 2 dans le cas d'un cétose.
Le pont oxydique formé partira toujours du carbone anomérique et peut relier ce dernier au troisième carbone suivant ou au quatrième carbone suivant.
Deux types de cycles peuvent donc être formés. Un cycle contenant 4 éléments carbones et un élément oxygène ou alors un cycle contenant 5 éléments carbones et un élément oxygène.
Par analogie avec des noyaux chimiques, on parlera de forme furane dans le premier cas (cycle constitué de 4 carbones et 1 oxygène) et de forme pyrane dans le second cas (cycle constitué de 5 carbones et 1 oxygène).
Lorsque le carbone anomérique forme un pont oxydique avec un carbone asymétrique, la position du groupement hydroxyle présent sur le carbone asymétrique induira la représentation du cycle du
même coté.
Lorsque le carbone anomérique forme un pont oxydique avec le dernier carbone de la chaîne (non asymétrique), le cycle est dessiné à droite s'il s'agit d'un composé de la série D et à gauche s'il s'agit d'un composé de la série L.




 !
!