Inscription / Connexion Nouveau Sujet
Chimie: acide et base
Bonjour j'ai une question concernant la théorie des acide et base quelqu'un peu m'aider svp
1)Est ce que le kb doit être suffisamment faible pour négliger le concentration en acide conjuguée?
2)la concentration de la base faible doit être suffisamment faible pour négliger le concentration en ions hydroxyde ?
Quelqu'un aurai synthése qui explique bien ?
Merci d'avance
Bonsoir
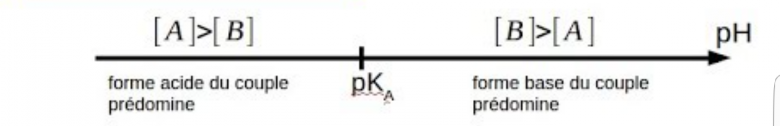
La notion de diagramme de prédominance, si elle est bien comprise, synthétise très bien le problème...
la concentration de la base faible doit être suffisamment faible pour négliger le concentration en ions hydroxyde ? Oui
Mais pour la 2
Est ce que le kb doit être suffisamment faible pour négliger le concentration en acide conjuguée? Justement Est ce que le kb doit être suffisamment élevé
@vanoise peux tu rectifier ?
Peux-tu exposer avec précision ton problème. Déterminer le pH d'une solution de base faible de concentration C ? Autre chose ?
Dans quel contexte exactement poses-tu ces questions : détermination du pH d'une solution de base faible ? Autre problème ?
Telles quelles, tes questions ne sont pas assez précises.
Il s'agit donc de la formule approchée donnant le pH d'une solution de base faible de concentration Cb. La démonstration nécessite plusieurs hypothèses simplificatrices :
1° : l'influence de l'autoprotolyse de l'eau doit être négligeable. Cela n'est vrai que si le pH obtenu est supérieur à 7,5.
2° : la réaction de la base sur l'eau doit avoir un taux de réaction très faible. Le pH doit donc appartenir au domaine de prédominance de la base faible, ce qui n'est vrai que si le pH obtenu est supérieur à (pKa+1)
Vous me comprenez pas vanoise
Cette question concerne la determination du pH a partir des constantes d'acidité, basicité


