Inscription / Connexion Nouveau Sujet
calcul masse volumique dun gaz
Bonjour a tous
je voudrais savoir comment on fait pour calculer la masse volumique a partir de la composition molaire d'un gaz qu'on va supposer parfait voici un exmple
C1 = 88,29 % mol
C2 = 7,70 % mol
C3 = 1,12 % mol
i - C4 = 0,08 % mol
n - C4 = 0,10 % mol
i - C5 = 0,02 % mol
n - C5 = 0,01 % mol
C6+ = 0,01 % mol
CO2 = 1,56 % mol
N2 = 1,06 % mol
He = 0,05 % mol
merci d'avance
Edit Coll : forum modifié
Salut,
Je ne suis plus un grand expert en matière de chimie.
Je me demande si on peut repartir de la loi des gaz parfaits :
P.V = n.R.T = m/M.R.T
<=> µ = m/V = P.M/R.T
avec au moins M = masse molaire du gaz = 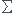 xi.Mi
xi.Mi
xi % pourcentage du gaz considéré
Mi sa masse molaire
Et en se penchant sur les pressions partielles de chaque gaz.
Dans l'attente de l'avis d'un chimiste 
je suis d'accord avec la formule indiquée par gbm.
 =P*M/(R*T)
=P*M/(R*T)
si M est exprimé en kg/mol on trouve  en kg/m3
en kg/m3
exemple dans le cas d'une composition approximative de l'air (20% O2 et 80% N2)
M= 0,80*28 +0,20*32 = 29g/mol = 29.10-3kg/mol
 dans les conditions normales de P et T
dans les conditions normales de P et T
 =29.10-3 *101325/(8,31*273)=1,3 kg/m3
=29.10-3 *101325/(8,31*273)=1,3 kg/m3
bonjour gbm.
Je suppose qu'il y a un mélange d'hydrocarbures ,entre autres.
j'ai donné une réponse niveau lycée ,c'est à dire que j'utilise le modèle des gaz parfaits.
Je ne maîtrise pas les situations plus complexes.

 .
.
