Inscription / Connexion Nouveau Sujet
Calcul du nombre de masse
Bonjour,
Je rencontre un souci dans l'exercice suivant :
Le Rubidium, dont la masse atomique est égale à 85,4677 g.mol-1 est composé de deux isotopes stables. Sachant que le nombre de masse de l'un des isotopes est supérieur de 2 unités au nombre de masse de l'autre isotope, identifier ces isotopes à l'aide des données ci dessous :
isotope => (A)Rb ; nombre de masse => ? ; abondance => 72.17%
isotope => (A+2)Rb ; nombre de masse => ? ; abondance => 27.83%
A = nombre de masse
Personnellement, j'arrive à une seule équation à 2 inconnues, ce qui est impossible à trouver à moins d'avoir un systèmes de 2 équations...
Quelqu'un a-t-il une idée ? Merci
Salut,
on a une approximation qui nous dit que, pour un isotope de nombre de masse Ai et d'abondance xi,
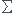 xi.Ai = M
xi.Ai = M
donc ici,
0,7217.A + 0,2783.(A+2) = 85,4677
donc A = .......


