Inscription / Connexion Nouveau Sujet
Acidité cyanophénol
Bonsoir,
Je suis assez embêté par un problème de chimie et j'aurai besoin d'un second avis.
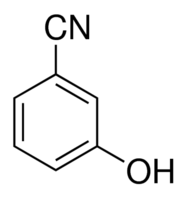
Je cherche à classer par ordre d'acidité croissant des composés, notamment le cyanophénol en différentes positions (ortho meta et para)
Je n'ai pas de mal à démontrer par effets mésomères que le cyanure situé en ortho et para ont des effets -M qui stabilisent la base conjuguée, les rendant plus acide que le phénol.
Cependant pour le groupement cyanure en meta, il n'y a pas de conjugaison directe avec l'oxygène chargé négativement de la base conjuguée. Le raisonnement que j'ai donc utilisé pour dire que l'effet mésomère est plus important (par rapport au phénol) est que la délocalisation engendrée par le cyanure entraine la formation d'un carbocation dans le cycle, qui a un effet -M plus important que le cycle sur l'oxygène de la base conjuguée.
Cependant je ne sais pas à quel point ce raisonnement est rigoureux (notamment si un carbocation est plus attracteur qu'un cycle). En effet, même s'il semble fonctionner par rapport aux valeurs de PKa que j'ai, on pourrait tout aussi bien dire que le cyanure délocalise les doublets du cycle et les rend moins accessible pour l'oxygène négatif...
Si quelqu'un connait donc la subtilité de raisonnement je suis preneur
Je vous souhaite une très bonne soirée.