Inscription / Connexion Nouveau Sujet
acide et metaux
bonjours
On donne les masses molaires en g/mol :M(C) = 12 ; M(H) = 1 ; M(Zn) = 65 ; M(S) = 32 ; M(O) = 16
Dans un ballon contenant 3,25 g de zinc pur, on verse 250 mL d'une solution d'acide sulfurique de concentration molaire 0.08mol/L.
1.Ecrire l'équation bilan de la réaction à froid entre l'acide sulfurique dilué et le zinc.
2.Montrer que toute la masse de zinc ne réagit pas.
3.Calculer la masse de sulfate de zinc formé.
4.calculer la masse de zinc réagit
5.En déduire la masse restante
Ma solution
1.
Zn + H2SO4  ZnSO4 + H2
ZnSO4 + H2
2.
montrons que la masse de zinc n'a pas totalement réagit
n(Zn)=3.25/65=0.05mol
n(H2SO4)=cv=0.25*0.08=0.02mol
d'aprés la reaction, une mol de zinc reagit avec une mol de H2SO4
or n(Zn)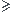 n(H2SO4) donc le zinc n'a pas totalement reagit
n(H2SO4) donc le zinc n'a pas totalement reagit
3.
n(H2SO4)=n(ZnSO4)=0.02mol=m/M donc m(ZnSO4)=0.02*98=1.96gramme
4.
n(Zn)réagit =0.02mol=m/M donc m(Zn)=0.02*65=1.3gramme
5.
La masse restante =3.25-1.3=1.95gramme
verifiez ma resolution s'il ya des erreurs et merci

 !
!

