Inscription / Connexion Nouveau Sujet
Acide base questions sur un exo
Bonjour, est ce que quelqu'un pourrait m'aider pour répondre aux questions 13,14,15 de l'exo suivant s'il vous plait j'ai mis un lien vers l'exercice (qui s'appelle partie D) et vers les données utiles
***Lien supprimés***
Merci d'avance.
Bonjour
Pour la clarté du forum et pour faciliter le référencement des sujets par les moteurs de recherche, le règlement du forum demande de recopier ici les cinq premières lignes du sujet et de proposer un seul problème par sujet ouvert.
ok alors je ne comprends pas comment repondre a:
Tracer une échelle des 𝑝𝐾𝑎 en repérant les espèces présente à chaque ajout de goutte titrante avant
l'équivalence.
j'ai depose l'image de l'exo car il y a un graph.
Kerlingss
ok alors je ne comprends pas comment repondre a:
Tracer une échelle des 𝑝𝐾𝑎 en repérant les espèces présente à chaque ajout de goutte titrante avant
l'équivalence.
j'ai depose l'image de l'exo car il y a un graph.
Kerlingss
ok alors je ne comprends pas comment repondre a:
Tracer une échelle des 𝑝𝐾𝑎 en repérant les espèces présente à chaque ajout de goutte titrante avant
l'équivalence.
j'ai depose l'image de l'exo car il y a un graph.

Il n'est pas nécessaire de faire une image du sujet. La référence précédente aurait suffit à condition de recopier les cinq premières lignes pour faciliter le référencement par les moteurs de recherche (Google ou autres...)
Commence par recopier les cinq premières lignes de l'énoncé...
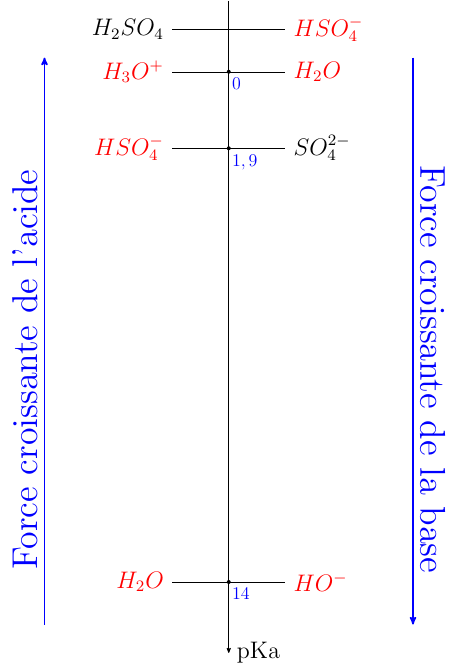
La première acidité de H2SO4 étant forte, les couples à prendre en compte sont H3O+/H2O, HSO4-/SO42- et H2O/HO-
Tu connais les pKa. Tu peux donc tracer le diagramme des pKa et envisager les réactions prédominantes lors du dosage. Le raisonnement est analogue à celui fait sur mon document.
ok merci.
Pour la question: 15. La simulation du titrage ne donne à voir qu'un seul saut de 𝑝𝐻. On en déduit alors que les 2 réactions
précédentes ont lieu simultanément. Ecrire alors l'équation-bilan de la réaction du titrage.
on obtient: H3O+ + HO- ⇌ 2 H2O
HSO4- + HO- ⇌ SO4 2- + H2O
l'equation bilan donne la somme des 2 ?? Merci d'avance.
Sans les cinq première lignes recopiées...
Le diagramme de prédominance conduit logiquement à ces deux équations...
Sont-elles quasi totales ?
Pourquoi peut-on les considérer comme simultanées plutôt que successives ?
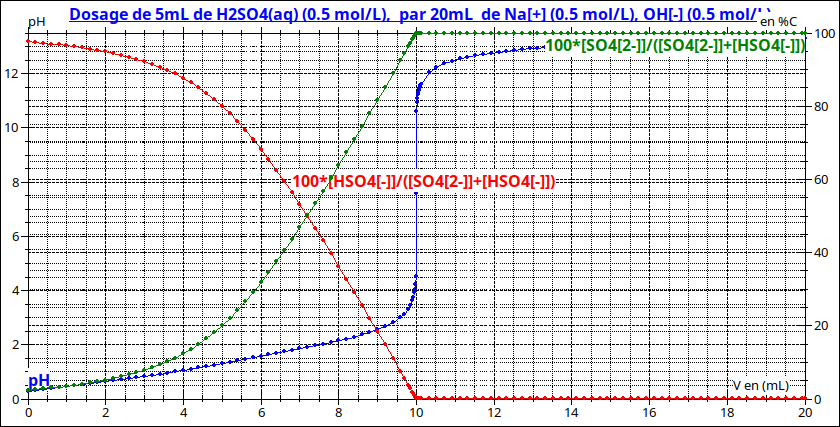
Tu peux aussi t'aider des courbes 2 et 3.
Inutile à mon avis de faire le bilan des deux...
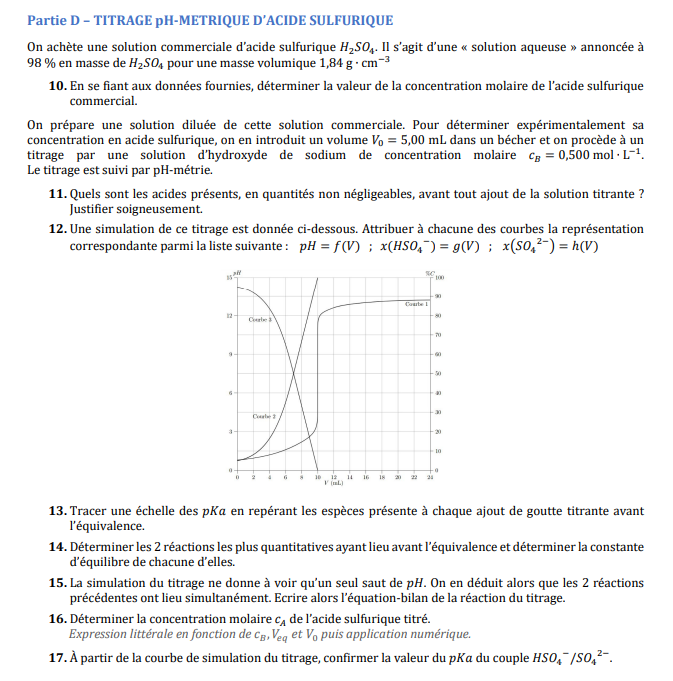
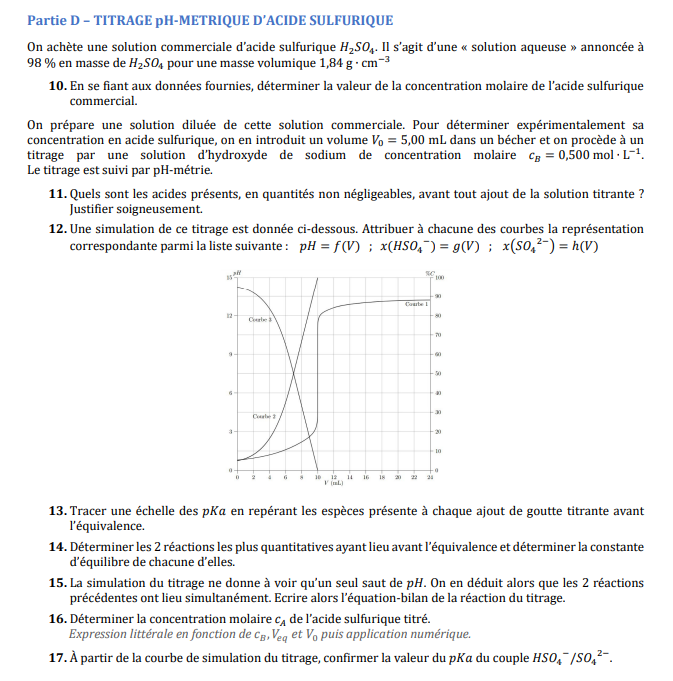
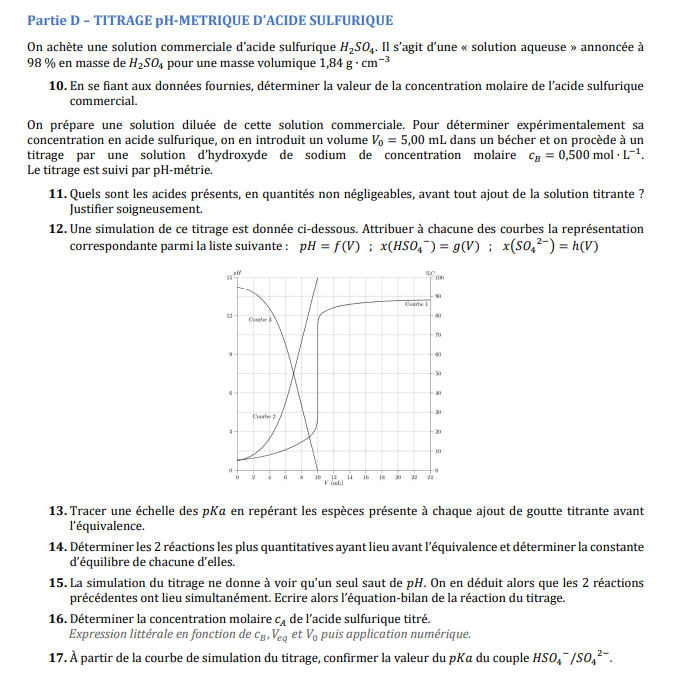
On achète une solution commerciale d'acide sulfurique 𝐻2𝑆𝑂4. Il s'agit d'une « solution aqueuse » annoncée à
98 % en masse de 𝐻2𝑆𝑂4 pour une masse volumique 1,84 g ∙ cm−3
10. En se fiant aux données fournies, déterminer la valeur de la concentration molaire de l'acide sulfurique
commercial.
On prépare une solution diluée de cette solution commerciale.
Merci mais je crois que le couple que vous avez mis tout en haut est en dessous du couple H3O+/H2O non ?
En fait j'ai besoin de connaitre la reaction totale car on me la demande et on doit l'utiliser pour repondre a la 16. (Déterminer la concentration molaire 𝑐𝐴 de l'acide sulfurique titré.
Expression littérale en fonction de 𝑐𝐵, 𝑉𝑒𝑞 𝑒𝑡 𝑉0 puis application numérique.)
Merci.
Le but du problème est d'obtenir la concentration apportée ca en acide sulfurique, c'est à dire la quantité de H2SO4 introduite par litre de solution.L'équation bilan demandée par l'énoncé est sans doute celle faisant intervenir directement H2SO4 et les ions hydroxyde de la solution de soude même si les molécules H2SO4 n'existent pas dans l'eau.
H2SO4 étant un acide fort, le pKa du couple H2SO4/HSO4- est négatif. C'est ce que rappelle mon diagramme.
On achète une solution commerciale d'acide sulfurique 𝐻2𝑆𝑂4. Il s'agit d'une « solution aqueuse » annoncée à
98 % en masse de 𝐻2𝑆𝑂4 pour une masse volumique 1,84 g ∙ cm−3
10. En se fiant aux données fournies, déterminer la valeur de la concentration molaire de l'acide sulfurique
commercial.
On prépare une solution diluée de cette solution commerciale.
Je ne vois pas du tout a quoi ressemble l'equation bilan du titrage si j'ai faux...
Personnellement, je ferais intervenir tes deux réactions de dosage mais aussi la réaction totale de H2SO4 sur l'eau. Cela correspond au bilan de ces trois réactions :
Les réactions 2 et 3 sont quasi totales compte tenu de leurs constantes d'équilibre très supérieures à l'unité.


