Inscription / Connexion Nouveau Sujet
Transfert thermique
Bonjour à tous, j'ai un exercice qui me pose problème, le voici :
Dans un calorimètre adiabatique, on introduit de l'au dont la masse est m1= 125g à une température T1= 19°C.
On ajoute par la suite un glaçon dont la masse est m2= 6g à une température T2= 0°C.
La température finale du mélange est T3= 14.4°C.
Déterminer la chaleur latente de fusion L fus du glaçon sachant que dans le cas présent on a : 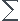 Qi=0
Qi=0
Données: c eau= 4.18 J.g.K.
Q th= m*c eau* t
t
Q fus= L fus* m
Toute aide sera la bienvenue, merci d'avance !
m1 * c eau * (T3 - T1) + m2 * L + m2 * ceau (T3 - T2) = 0
En unités SI :
0,125 * 4180 * (14,4 - 19) + 0,006 * Lfus + 0,006 * 4180 * (14,4 - 0) = 0
Lfus = 3,4.10^5 J/kg
-----
Recopier sans comprendre est inutile. 
Salut,
Regarde mon explication dans le cas où il n'y a pas de changement de phase :
![]() Clou
Clou
On attend tes propositions

Je n'ai pas compris, et oui recopier serait inutile..
je ne comprends pas comment on passe de ça : Q th= m*c eau*t
A ça : m1 * c eau * (T3 - T1) + m2 * L + m2 * ceau (T3 - T2) = 0
Et puis, c'est quoi la chaleur latente de fusion ?
Et gbm, merci pour l'autre topic, je l'ai lu, mais je n'arrive pas à faire le lien avec mon problème..


