Inscription / Connexion Nouveau Sujet
Transferts thermiques
Dans un calorimètre adiabatique, on introduit de l'eau dont la masse est m1= 200g a une température de T1= 21°C.
On ajoute par la suite de l'eau dont la masse est m2= 150g à une température de T2= 53°C.
1) Expliquer ce qu'implique d'utiliser un calorimètre adiabatique.
2) Déterminer la température finale T3 du mélange obtenu.
Dans le cas présent on a : 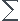 Qth= 0.
Qth= 0.
Données: C eau= 4.18 J.g.K
Q th= m*c eau * t
t
Pour la calorimètre adiabatique, je sais que c'est un appareil qui mesure les échanges de chaleur et que c'est un isolant thermique parfait.
Pour le calcul en revanche, je ne sais pas du tout comment faire, donc tout aide serait la bienvenue, merci d'avance.



