Inscription / Connexion Nouveau Sujet
Site accepteur de doublet d'électrons et H-
Bonjour .
1. Donner la représentation de Lewis des espèce suivantes :
a. cation méthyle H3C+ ;
b. fluorométhane H3CF ;
c. méthanal H2CO.
2. Dans les espèces b et c , les liaisons polarisées sont respectivement C-F et C=O. Sur les représentations de Lewis , faire apparaître en les justifiants , les charge partielles sur les atomes de ces liaisons.
3. Identifier le site accepteur de doublet d'électrons présent dans chacune des trois espèces de la question 1.
4. Relier par une flèche courbe rouge le site donneur de H- avec le site accepteur de ces trois espèces.
5. Dans quelle(s) espèce(s) le carbone ne vérifie-t-il pas la règle de l'octet?
1 et 2 .
3.site accepteur : je ne sais plus si c'est l'atome avec une charge positive qui est le site accepteur ou c'est celui qui est négatif .
mais j'ai dis : molécule 1: site accepteur : je ne sais pas car le carbone a déjà un double non liant donc il ne peut plus en accepter . est-ce possible qu'il est un doublet non liant car j'ai vue que normalement non .
molécule 2: site accepteur : carbone .
molécule 3: site accepteur : carbone mais je ne suis pas sûr .
4; j'ai fais une flèche courbe que pour la 3eme molécule . et je les fait partir du H- et allant jusqu'au carbone .
5. dans aucune des molécules la rège de l'octet est respecté .
merci d'avance .
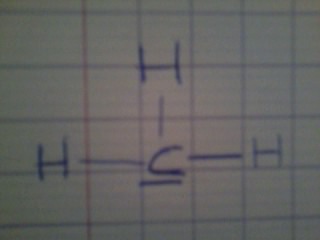
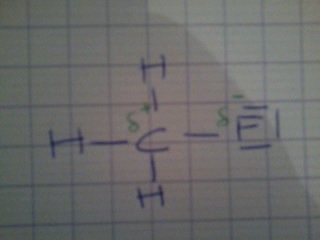
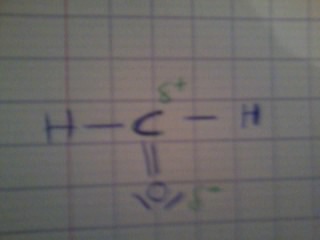
salut  !
!
1 et 2 ce sont les images je présume. Pour la première tu oublies la charge. Pour les deux autres c'est bon
3) Un site donneur de doublet d'électrons est le lieu d'une espèce chimique qui présente un excès de charges négatives
5) justifie
pour la 1 il ne demande pas de mettre les charges c'est pour ça que je ne les ai pas misent .
mais sinon j'aurais mis un delta moins sur la carbone et des delta + sur les hydrogènes .
3. a ok . donc le site accepteur est le carbone .
pour la molécule 2 la flèche il faut la faire du fluor jusqu'au carbone alors ? car le fluor vue qu'il est négatif il va passer un de ses doublets non liant .
5. car dans chaque molécule le carbone est le site accepteur et il vérifie déjà la règle de l'octet donc en lui ajoutant un doublet non liant de l'hydrogène sa lui fait plus de 8 électrons .
Au temps pour moi je pensais que tes dessins couvraient les deux premières questions
3) oui 
4) l'ion hydrure va venir "se greffer" sur le carbone. Donc en réalité tu as la liaison C-F qui se transforme en doublet non liant pour le fluor.
autour du H- il y a un doublet non liant et donc sa fait qu'il va se coller au carbone . je pensais qu'il lui donner juste son doublet non liant .
Il est plus probable que le carbone cherche davantage à s'entourer de 4 atomes d'hydrogène. Le fluor est très électronégatif et à tendance à "s'échapper" lors de ce type de réactions.
Pour ta dernière question c'est ok
ok .
pour la molécule 1 la flèche courbe va du H- vers le carbone mais il faut faire une autre flèche en bleu pour faire en sorte que la règle de l'octet soit respecter .
Nan il ne peut pas porter de doublet  Mais le doublet non liant devient la liaison partagée entre H et C
Mais le doublet non liant devient la liaison partagée entre H et C
le H et C avait tout deux un doublet non liant .
donc si ce n'est pas le H qui en a un après leur réunification c'est le C qui en a un .


