Inscription / Connexion Nouveau Sujet
Ester
s'il vous plaît aidez-moi!
7,4 g d'ester est obtenu par la réaction entre un monoalcool saturé et le chlorure de propanoyle. Le rendement de la réaction est de 70%.
1. Écrire l'équation de cette réaction.
2. Identifier la vraie formule de monoalcool.
3. Calcul de la masse de chlorure de propanoyle qui a besoin d'utiliser dans cette réaction.
Ils donnent: M (monoalcool) = 46 g / mol, M (ester) = 102 g / mol
bonjour,
il s'agit d'une réaction d'estérification qui met en jeu un alcool R-OH et un chlorure d'acide dont tu peux écrire la formule.
On obtient un ester et HCl.
Revois ton cours pour ce type de réaction.
L'ester aura comme formule CH3-CH2-COO-R
R est de la forme Cx H(2x+1)- (radical alkyle)
or M(alcool)=46g/mol
on peut en déduire x ,et la formule de l'alcool.
la masse d'ester obtenue est 7,4 g lorsque le rendement 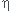 est 70% (0,70)
est 70% (0,70)
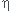 =masse réellement obtenue/masse théorique
=masse réellement obtenue/masse théorique
la masse théorique correspond à la masse obtenue si la réaction était totale.
Tu peux ainsi calculer la masse théorique d'ester que l'on aurait obtenue si la réaction était totale ,puis la qté de matière correspondante.
L'équation montre qu'il faut 1 mol de chlorure d'acide pour obtenir 1 mol d'ester.
La qté de chlorure d'acide est donc égale à la qté d'ester max calculée précédemment.
On en déduit alors m(Chlorure d'acide)
Merci baucoup,
Je suis désolé. l'exercice est la suivante:
7,4 g d'ester est obtenu en faisant réagir entre 4,6 monoalcool saturé et de chlorure de propanoyle. Le rendement de la réaction est de 70%.
1. Écrire l'équation de cette réaction.
2. Identifier la vraie formule de monoalcool.
3. Calcul de la masse de chlorure de propanoyle qui a besoin d'utiliser dans cette réaction.
Ils donnent: M (monoalcool) = 46 g / mol, M (ester) = 102 g / mol
Je pense:
1.CH3CH2COCl + R-OH ---> CH3CH2COO-R + HCl
2.Monoalcool sature: M(CnH2n+1OH) = 46 g/mol => C2H5OH
3.Il est diffucult pour moi.
7,4 g d'ester est obtenu en faisant réagir entre 4,6 monoalcool saturé et de chlorure de propanoyle.
je suppose qu'on fait réagir 4,6 g d'alcool soit 0,1 mol
j'avoue ne pas comprendre ce problème :
Puisque la réaction se fait mol à mol(une mol d'alcool réagit avec une mol de chlorure d'acide) ,un rendement de 70 % correspond à 70% du réactif limitant .
on obtient n(ester )=7,4/102=0,0725 mol
La qté de réactif limitant devrait être n=0,0725/0,70=0,103 mol
Or on n' a que 0,10 mol d'alcool.
Au mieux on obtiendrait 0,10 mol d'ester.
Il y a quelque chose qui ne va pas dans cet énoncé
Il y a quelque chose qui ne va pas dans cet énoncé
J'aurais du dire il y a quelque chose que je ne comprends pas dans cet énoncé.
je reprends une partie d'un post précédent:
rendement=masse réellement obtenue/masse théorique ou qté réellement obtenue/qté théorique
la masse théorique correspond à la masse qui serait obtenue si la réaction était totale.Celle -ci dépend du réactif limitant.
or on obtient n=7,4/102=0,0725 mol d'ester avec un rendement de 70%
si la réaction avait été totale on aurait obtenu n=0,0725/0,70=0,104 mol d'ester soit environ 0,1 mol.
d'après ton énoncé ,on utilise 0,1 mol d'alcool.(n=4,6/46)
L'alcool est donc le réactif limitant.
Il ne peut pas y avoir moins de 0,1 mol de chlorure d'acide ,car dans ce cas,la qté théorique d'ester serait inférieure à 0,1 mol.Or elle vaut 0,1mol.(0,104 mol)
Cependant ,je ne vois pas ce qui permet de calculer la qté de chlorure d'acide mis en jeu autrement que de dire qu'elle est supérieur ou égale à 0,1 mol.
Pour connaître la qté de chlorure ,il faudrait connaître la constante de réaction K
Quelque chose m'échappe.Autrement dit,il y a quelque chose que je ne comprends pas.
Cher coriolan,
Je pense que l'exercice a erreur.
Pourrais-je avoir votre adresse e-mail?
sincèrement
Selon moi je ne pense pas qu'il y a une erreur dans l'exercice . En effet la première et deuxième question ne posent aucun problème ce n'est que la dernière question qui reste à répondre. Cependant nous connaissons le nombre de mole de chaque molécule concernant puis la réaction se fait mole à mole avec un rendement égale à 0.7 donc en posant 0.7x m/M =n ester avec m/M la quantité de matière du chloryre de propyle on trouvera la masse demandé


