Inscription / Connexion Nouveau Sujet
titrage de l'acide lacyique dans un alit
Bonjours, j'étais en train de regarder mon livre de physique chimie quend je suis tombée sur cet exo, du coup j'ai voulu le faire et je bloque à une question, l'énoncé est:
On introduit dans un erlenmeyer vA=20,0 mL d'un échantillon de lait. On ajoute progressivement une solution d'hydroxyde de sodium de concentration cb= 5,0 10-2 mol/L.
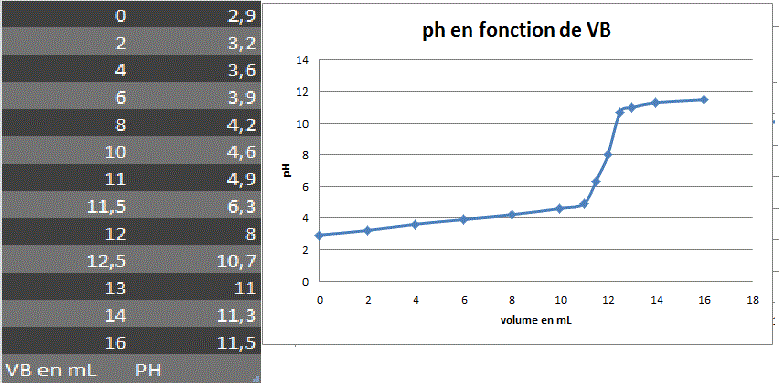
on obtient les résultas suivants (tableau)
on note l'acide HA et la base A-
les données sont: H2O(l)/ HO-(aq), pKa=14.0
H3O+(aq)/ H2O(l), pKa=0.0
HA(aq)/A-(aq), pKa=3.9
masse molaire de l'acide lactique: M(HA)=90.0 g/mol
j'ai mis que l'équation était AH(aq)+ HO-(aq)  (double fleche) A-(aq) +H2O(l)
(double fleche) A-(aq) +H2O(l)
la question est: pour quel volume de soude versé, noté Vs; les espèces HA(aq) et A-(aq) sont elles présentes en quantité égale dans le bécher?
reponse: j'avais trouvé 6ml en utilisant la formule pH=pKa+ log(A-/AH). mais je n'en suis absolument pas sur.
lorsque [AH]=[A-],la moitié de la qté d'acide a été transformée en sa base conjuguée.
On est à la 1/2 équivalence.
détermine graphiquement le volume de OH- versé à l'équivalence (méthode des tangentes).Pour la moitié de ce volume on est à la 1/2 équivalence
Autre méthode:
lorsque [A-]=[AH} pH=pKa
comme on connait le pKa ,il suffit de repérer graphiquement pour quel volume de OH- versé on a PH=pKa
Ce volume est voisin de 6mL


